题目内容
把相同体积、相同质量分数的稀盐酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如图所示.这三种金属的活动性顺序为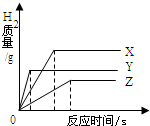 如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为
如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为分析:根据图象我们可以得出,在单位时间内产生氢气的速度是Y>X>Z.正好与金属活动顺序相一致,金属活性越高的,产生氢气速度越快.因此可知三种金属的活动顺序.通过刚才的分析我们发现,假如X、Y、Z都是+2价金属,在质量相等时与酸反应,相对原子质量越小的,产生的氢气质量也越多,因此可知相对原子质量由大到小的顺序.
根据题意书写一氧化碳与氧化铁、稀盐酸与氧化铁的化学方程式.
根据题意书写一氧化碳与氧化铁、稀盐酸与氧化铁的化学方程式.
解答:解:根据图象我们可以得出,在单位时间内产生氢气的速度是Y>X>Z.也就是说Y与酸反应的速度最快,X次之,Z最慢,正好与金属活动顺序相一致,金属活性越高的,产生氢气速度越快.因此三种金属的活动顺序为Y>X>Z.通过刚才的分析我们发现,假如X、Y、Z都是+2价金属,在质量相等时与酸反应,相对原子质量越小的,分子数量(摩尔数mol 分子的量)越多,产生的氢气质量也越多,因此相对原子质量由大到小的顺序为Z>Y>X.
沙土中含有丰富钛铁矿,主要成分为TiO2、Fe2O3等,若用CO还原这种矿石,其中生成铁的化学方程式为:3CO+Fe2O3
2Fe+3CO2;用稀盐酸清洗铁钉表面的铁锈(主要成分是Fe2O3),其化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O,该反应的反应类型是复分解反应.
故答为:Y>X>Z,Z>Y>X;3CO+Fe2O3
2Fe+3CO2;Fe2O3+6HCl=2FeCl3+3H2O;复分解反应
沙土中含有丰富钛铁矿,主要成分为TiO2、Fe2O3等,若用CO还原这种矿石,其中生成铁的化学方程式为:3CO+Fe2O3
| ||
故答为:Y>X>Z,Z>Y>X;3CO+Fe2O3
| ||
点评:本题主要考查了铁的冶炼原理;还考查了铁的冶炼原理的有关化学方程式的书写;掌握反应类型的判定方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
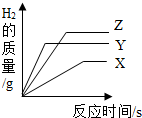 把相同体积、相同质量分数的稀盐酸,分别滴加到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如图所示.这三种金属的活动性顺序为
把相同体积、相同质量分数的稀盐酸,分别滴加到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如图所示.这三种金属的活动性顺序为


