题目内容
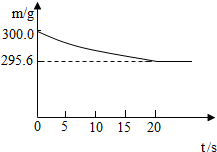 向盛有Na2CO3和NaCl固体混合物样品的烧杯中加入200g稀盐酸恰好完全反应,反应过程中用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示,回答下列问题.
向盛有Na2CO3和NaCl固体混合物样品的烧杯中加入200g稀盐酸恰好完全反应,反应过程中用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如图所示,回答下列问题.(1)完全反应后,产生二氧化碳气体质量
(2)混合物样品中Na2CO3的质量为
(3)参加反应的盐酸中溶质的质量分数是多少?(写出计算过程)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)氯化钠和碳酸钠的固体混合物与稀盐酸混合后,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,由于反应放出了二氧化碳,所以反应后烧杯及剩余物质的质量减小,减小的质量即为气体二氧化碳的质量;
(2)根据反应的化学方程式,利用生成气体二氧化碳的质量可计算原混合物中碳酸钠的质量;
(3)根据反应的化学方程式,利用生成气体二氧化碳的质量可计算参加反应的盐酸中溶质的质量,进而求出参加反应的盐酸中溶质的质量分数即可.
(2)根据反应的化学方程式,利用生成气体二氧化碳的质量可计算原混合物中碳酸钠的质量;
(3)根据反应的化学方程式,利用生成气体二氧化碳的质量可计算参加反应的盐酸中溶质的质量,进而求出参加反应的盐酸中溶质的质量分数即可.
解答:解:(1)根据质量守恒定律,反应生成二氧化碳气体的质量=300.0g-295.6g=4.4g;故填:4.4;
(2)设原混合物中碳酸氢钠的质量为x,参加反应的盐酸中溶质的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
x y 4.4g
=
x=10.6g
=
y=7.3g
故答案为:10.6;
(3)参加反应的盐酸中溶质的质量分数=
×100%=3.65%
答:参加反应的盐酸中溶质的质量分数是3.65%.
(2)设原混合物中碳酸氢钠的质量为x,参加反应的盐酸中溶质的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 44
x y 4.4g
| 106 |
| x |
| 44 |
| 4.4g |
x=10.6g
| 73 |
| y |
| 44 |
| 4.4g |
y=7.3g
故答案为:10.6;
(3)参加反应的盐酸中溶质的质量分数=
| 7.3g |
| 200g |
答:参加反应的盐酸中溶质的质量分数是3.65%.
点评:本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力,解题时要特别注意解题步骤的规范性,从而掌握通过已知计算未知的解题方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
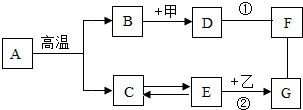 A~G是初中化学常见的物质,它们之间的关系如图所示,其中①是中和反应,乙是一种红色粉末.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题:
A~G是初中化学常见的物质,它们之间的关系如图所示,其中①是中和反应,乙是一种红色粉末.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题:


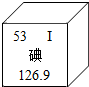 人体内约有50多种元素,其中碘元素是人体必需的微量元素.(1)碘元素的原子序数是
人体内约有50多种元素,其中碘元素是人体必需的微量元素.(1)碘元素的原子序数是