题目内容
【题目】实验中,小红误将氢氧化钠溶液当成酸滴加到金属铝中,结果发现也有气泡产生,为了解该气体的成分,实验小组进行了以下探究
(1)【提出猜想】小红猜想是氧气;小敏猜想是氢气;小雨猜想是二氧化碳
其他同学认为小雨的猜想是错误的,理由是;
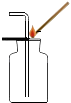
(2)【进行实验】利用图I所示的装置分别进行实验
小红:反应一段时间后,将带火星的木条放在a处,观察到 , 则她的猜想错误。
(3)小敏:①用图II所示装置干燥从a导管出来的气体,将管口a与(填“b”或“c“)端管口连接。
②反应一段时间,点燃干燥的气体,通过对现象的分析,得出他的猜想正确。
(4)【得出结论】铝和氢氧化钠反应生产氢气和偏铝酸钠(NaAlO2),
反应的化学方程式为: 。
(5)【交流讨论】有同学认为,小敏的实验方案有欠缺,步骤②中存在安全隐患,理由是。
(6)【反思提升】许多重大科学发现,源自对试验中异常现象的大胆质疑,深入研究。下列科学成果是通过对异常现象研究得出的是 (填序号)。
A.侯德榜潜心研究制碱技术发明了联合制碱法
B.拉瓦锡深入研究前人忽视的异常现象发现了氧气
C.张青莲主持测定了多种元素相对原子质量的新值
【答案】
(1)不符合质量守恒定律(或反应物中不含碳元素)
(2)木条不复燃
(3)b
(4)2Al+2NaOH+2H2O═2NaAlO2+3H2↑
(5)若氢气不纯,点燃可能发生爆炸
(6)B
【解析】【提出猜想】根据质量守恒定律可知,化学反应前后元素的种类不变。氢氧化钠溶液、金属铝中只有氢、氧、钠、铝四种元素,没有碳元素,不可能生成含有碳元素的二氧化碳气体;
【进行实验】(2)氧气有助燃性,能使带火星的木条复燃。木条不复燃 ,证明气体不是氧气。(3)C为了使被干燥的气体与干燥剂充分接触,将被干燥的气体应该长进短出,所以气体应从长管b导入浓硫酸中。
【得出结论】 铝和氢氧化钠溶液反应生成偏铝酸钠和氢气。
【交流讨论】可燃性气体中混有空气时,点燃可能发生爆炸,所以在点燃或加热可燃性气体前要先验纯。
【反思提升】普利斯特里(Joseph Priestley)在拉瓦锡之前发现了氧气,但由于受"燃素说"的影响,他把氧气当作了"燃素"。拉瓦锡正是在普利斯特里研究的基础上,破除了"燃素说"的束缚,确认氧气是由一种元素形成的纯净物。
故答案为:(1)不符合质量守恒定律(或反应物中不含碳元素);(2)木条不复燃;(3)b;(4)2Al+2NaOH+2H2O═2NaAlO2+3H2↑;(5)若氢气不纯,点燃可能发生爆炸;(6)B
【提出猜想】根据反应前后元素的种类不变作答
【进行实验】根据氧气能够支持燃烧和浓硫酸干燥气体气体从长管进入来解答
【得出结论】铝和氢氧化钠和反应生成偏铝酸钠和氢气
【交流讨论】根据氢气可燃,点燃易爆炸解答
【反思提升】根据研究成果分析