题目内容
【题目】实验室按下图所示装置制取CO2,并检验CO2的性质.试回答以下问题:
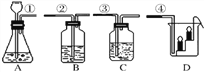
(1)实验开始前,先应检查装置A的______________。
(2)用装置A来制取CO2,所用的药品是__________和__________(写化学式)。
(3)若要用装置B鉴定CO2,在B中应盛放的试剂名称是__________,当将标①和②的导管口连接时,B中看到的实验现象是_______________。
(4)若要用装置C证明CO2能与水反应生成碳酸,C中除有少量水外,应加入的试剂是______________,当将标①和③的导管口连接时,C中看到的实验现象是__________________。
(5)烧杯D中放有燃着的蜡烛如上图所示,当将标①和④的导管口连接时,D中看到的实验现象是______________。
【答案】 气密性 CaCO3 HCl 石灰水 变浑浊 石蕊 石蕊有紫色变红色 蜡烛由下向上依次熄灭
【解析】试题分析:(1)制取气体实验开始前,要检查装置的气密性,防止装置漏气;(2)实验室制取二氧化碳的药品是大理石和稀盐酸,大理石的主要成分是碳酸钙,稀盐酸中发生反应的是盐酸,其化学式分别是CaCO3、HCl;(3)二氧化碳能使澄清的石灰水变浑浊,可用来检验二氧化碳,因此当将标①和②的导管口连接时,B中看到的实验现象是澄清的石灰水变浑浊;(4)CO2能与水反应生成碳酸,碳酸可使紫色石蕊试液变红,因此当将标①和③的导管口连接时,C中看到的实验现象是石蕊试液变红;(5)二氧化碳不能燃烧,也不能支持燃烧,密度比空气大,所以当将标①和④的导管口连接时,D中看到的实验现象是底下蜡烛先熄灭,上边的蜡烛后熄灭;

【题目】马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:
加入稀盐酸的质量/g | 生成气体的总质量/g | |
第1次 | 20 | 1.1 |
第2次 | 20 | 2.2 |
第3次 | 20 | m |
第4次 | 20 | 4.4 |
第5次 | 20 | 4.4 |
(1)m的值为_________g
(2)12g石灰石样品中碳酸钙的质量等于_________g
(3)反应完全后最终溶液中氯化钙的质量分数为_______?(写出计算过程,计算结果精确至0.1)