题目内容
下列图象分别与选项中的操作相对应,其中可能合理的是( )
|
分析:A、根据氢氧化钠溶液显碱性,其pH值>7进行解答;
B、根据碳酸氢钠和碳酸钠与稀盐酸反应的化学方程式可以完成解答;
C、根据镁和铁的金属的活动性顺序可以完成解答;
D、根据电解水的实验结论可以完成解答.
B、根据碳酸氢钠和碳酸钠与稀盐酸反应的化学方程式可以完成解答;
C、根据镁和铁的金属的活动性顺序可以完成解答;
D、根据电解水的实验结论可以完成解答.
解答:解:A、氢氧化钠溶液显碱性,其pH值>7所以开始pH值应该大于7,随着加入水,碱性变弱,pH值减小,但仍然显碱性,pH值不能降到7,故A错;
B、设碳酸钠和碳酸氢钠的质量均为1g,则:
NaHCO3+2HCl═NaCl+H2O+CO2↑
84 44
1g
gg
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
1g
gg
所以可以判断等质量的碳酸钠和碳酸氢钠,碳酸氢钠反应产生二氧化碳的质量要大,故B正确;
C、镁的活动性比铁强,所以反应速率要快,但是图中显示的是铁的反应速率快,故C错;
D、电解水实验中产生氢气和氧气的质量之比为1:8,故D错.
故选B.
B、设碳酸钠和碳酸氢钠的质量均为1g,则:
NaHCO3+2HCl═NaCl+H2O+CO2↑
84 44
1g
| 44 |
| 84 |
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 44
1g
| 44 |
| 106 |
所以可以判断等质量的碳酸钠和碳酸氢钠,碳酸氢钠反应产生二氧化碳的质量要大,故B正确;
C、镁的活动性比铁强,所以反应速率要快,但是图中显示的是铁的反应速率快,故C错;
D、电解水实验中产生氢气和氧气的质量之比为1:8,故D错.
故选B.
点评:熟练掌握酸碱盐的化学性质,能够熟练的运用金属的活动性顺序的应用来解答相关题目,知道电解水实验中氢气和氧气的体积比为2:1,而不是质量比.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列图象分别与选项中的操作相对应,其中可能合理的是( )
A、 将等质量的钠、镁、铝放入相同浓度、相同质量的稀硫酸中 | B、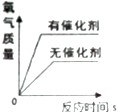 用相同浓度、相同质量的过氧化氢溶液来制取氧气 | C、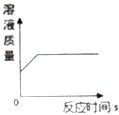 将一根铁钉放入一定质量的硫酸铜溶液中 | D、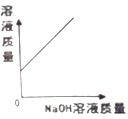 向一定质量的硫酸铜溶液中不断滴加NaOH溶液 |



