题目内容
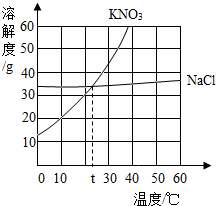 根据KNO3和NaCl的溶解度曲线,回答下列问题:
根据KNO3和NaCl的溶解度曲线,回答下列问题:(1)10℃时KNO3的溶解度
(2)t℃时,将mg KNO3、ng NaCl 分别溶解在20mL水中恰好饱和,则m
(2)下面是两同学分别提出的从海水中获取食盐的方法.甲:蒸发水 乙:冷却热饱和溶液 你认为
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用
专题:溶液、浊液与溶解度
分析:(1)根据物质的溶解度曲线可以判断某一温度时物质溶解度的大小比较;
(2)t℃时,硝酸钾和氯化钠的溶解度相等;
(3)从溶液中结晶的方法有两种:蒸发结晶和降温结晶,物质的溶解度受温度变化影响较小时,应该用蒸发结晶;物质的溶解度受温度变化影响较大时,应该用降温结晶.
(2)t℃时,硝酸钾和氯化钠的溶解度相等;
(3)从溶液中结晶的方法有两种:蒸发结晶和降温结晶,物质的溶解度受温度变化影响较小时,应该用蒸发结晶;物质的溶解度受温度变化影响较大时,应该用降温结晶.
解答:解:(1)10℃时KNO3的溶解度小于NaCl溶解度.
故填:<.
(2)因为t℃时硝酸钾和氯化钠的溶解度相等,将mgKNO3、ngNaCl分别溶解在20mL水中恰好饱和,说明则m和n相等.
故填:=.
(2)因为氯化钠的溶解度受温度变化影响很小,从海水中获取食盐最好利用蒸发水的方法.
故填:甲.
故填:<.
(2)因为t℃时硝酸钾和氯化钠的溶解度相等,将mgKNO3、ngNaCl分别溶解在20mL水中恰好饱和,说明则m和n相等.
故填:=.
(2)因为氯化钠的溶解度受温度变化影响很小,从海水中获取食盐最好利用蒸发水的方法.
故填:甲.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
下列化学基本实验操作中正确的是( )
A、 闻气体气味 |
B、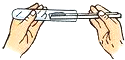 往试管内送入固体粉末 |
C、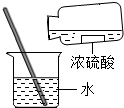 浓硫酸的稀释 |
D、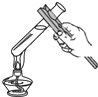 用酒精灯加热液体 |
如图是硫原子的原子结构示意图,下列对硫原子的叙述不正确的是( )
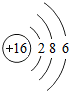
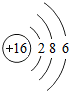
| A、硫原子第三电子层有6个电子 |
| B、硫原子核内有16个质子 |
| C、硫原子最外层电子的能量低于第二层电子的能量 |
| D、硫原子在化学反应中容易得到电子 |