��Ŀ����
����Ŀ��ijͬѧ�������ʵ�����Ʒ���������̽���������ͼ��Ҫ��ش��������⣺
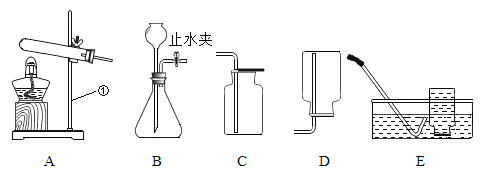
��1����������������______________
��2��װ��B��ij���������¶˱������뵽Һ����������������� _____________��
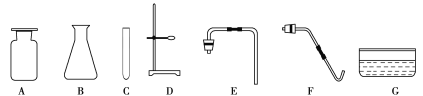
��3��ʵ�����ø��������ȡO2�ķ���װ����_______����ѡװ������ĸ��ʾ����ʵ��ʱ��װ��ҩƷ��������Ƥ��֮ǰ�IJ�����__________________������Eװ���ռ��������ѵ��ܷŵ�����ƿ�ڵ�����ʱ����___________________________��
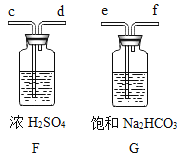
��4��ʵ������Bװ����ȡ������̼�Ļ�ѧ����ʽ_______________________________�����ƵõĶ�����̼�г�����ˮ�������Ȼ�������ʣ�Ϊ�õ����﴿���Ķ�����̼���壬��ʹ��װ��F��G��ȥ����Щ���ʣ�������ͨ��F��Gװ�ýӿڣ����ܿڣ�����ȷ����˳����_________________��
��5��ij��ȤС������ʵ������CO2�ķ�Һ�õ�CaCO3��NaCl���壬�������£�
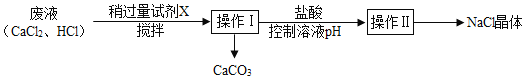
�� �Լ�X����___________��ѡ����ţ���
A NaOH��Һ b K2CO3��Һ c Na2CO3��Һ d Ba(NO3)2��Һ
�� �Լ�XҪ���Թ�����Ŀ����_______________________________________.
�� ����I��Ҫ�õ��IJ��������в�������______���ձ����ڲ���IIǰ������Һ��pH��ʵ�ʲ����У��ɿ��Ƶ�pHΪ_______��
���𰸡�����̨ ����©�� A ���Թܿڷ�һ���� ������������ð��ʱ CaCO3+2HCl�TCaCl2+H2O+CO2�� e��f��c��d c �����Ȼ��� ©�� ��7
��������
��1��������������̨��
��2��װ��B�г���©�����¶˱������뵽Һ���
��3�����ȹ�����ȡ���壬ѡ����װ��A����ʵ�����ø��������ȡO2�ķ���װ����A��ʵ��ʱ��װ��ҩƷ��������Ƥ��֮ǰ�IJ��������Թܿڷ�һ�������Է�������ض��������ܣ�����Eװ���ռ���������������������ð��ʱ��ʼ�ռ�����ʱ�Ǵ�����������
��4��ʵ�����ô���ʯ��ϡ������ȡ������̼������ʯ��Ҫ�ɷ���̼��ƣ���Ӧ�Ļ�ѧ����ʽΪ��CaCO3+2HCl=CaCl2+H2O+CO2�������ƵõĶ�����̼�г�����ˮ�������Ȼ�������ʣ���������к��ж����������ʣ�����һ����ˮ����������ȥˮ������ϴ��װ�õĵ������dz����̳���������ͨ��F��Gװ�ýӿڣ����ܿڣ�����ȷ����˳����e��f��c��d��
��5���� ��ʵ��Ŀ���ǵõ�CaCO3��NaCl���壬˵����Ӧ�м�����̼������ӣ�Ϊ�˲������������ӣ����Լ�Xֻ����Na2CO3��Һ��Na2CO3+CaCl2 =CaCO3��+2NaCl����ѡc���� �Լ�XҪ���Թ�����Ŀ���dz���̼���ơ��� ͨ�����˿ɽ�������ˮ�Ĺ���������Һ����룬�ʲ���I�ǹ��ˣ�������Ҫ�õ��IJ��������в�������©�����ձ���̼������Һ�Լ��ԣ����������Ŀ���dz�ȥ̼���ƣ��ڲ���IIǰ������Һ��pH��ʵ�ʲ����У��ɿ��Ƶ�pHΪ��7����������Թ���������ʱ���ɳ�ȥ��

 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д�����Ŀ�������±�����ʵ�飬�й�˵���������������
������KOH��Һ�еμ�CuSO4��Һ | ������BaCl2��Һ�еμ�CuSO4��Һ | |
���� | �� | ��ɫ���� |
��ѧ����ʽ | 2KOH + CuSO4 =Cu(OH)2��+ K2SO4 | �� |
A. ������ɫ����
B. �ڷ�Ӧ�Ļ�ѧ����ʽΪCuSO4 +BaCl2 =BaSO4��+CuCl2
C. ������Ӧ�����ڸ��ֽⷴӦ
D. ֻҪ�г������ɵķ�Ӧ�����ڸ��ֽⷴӦ