题目内容
现有3g某金属样品(杂质不与酸反应,也不溶于永),与l00克质量分数19.6%的稀硫酸恰好完全反应,过滤,将得到的硫酸盐溶液蒸干,得到21.9g固体。则该金属样品中金属的质量分数为( )
| A.90% | B.60% | C.75% | D.50% |
A
试题分析:根据题意恰好完全反应,则所得固体的质量为,硫酸的质量加金属的质量减去产生氢气的质量,100g19.6%的稀硫酸中含氢元素的质量为:100g*19.6%*2/98=0.4g,所以原样品中金属的质量为:21.9g+0.4g-19.6g=2.7g,所以该金属样品中金属的质量分数为2.7g/3g*100%=90%。故选A。

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
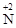
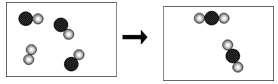
 ”和“
”和“  ” 表示不同元素的原子。下列说法正确的是
” 表示不同元素的原子。下列说法正确的是
 ”和“
”和“  ”分别表示碳原子和氧原子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如下:
”分别表示碳原子和氧原子,这两种元素组成的化合物在一定条件下能发生以下反应,反应前后的微观模拟图如下: