题目内容
某小组同学在学习镁条与盐酸反应会放出大量热的实验后,想研究金属铝与盐酸反应是否也放热,同学们设计了如图所示实验,请你和该小组同学共同完成实验。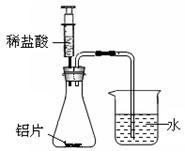
将注射器中的稀盐酸加入到锥形瓶内时,可观察到锥形瓶中产生的现象为 ;
甲同学观察到反应一段时间后,导管口有气泡冒出的现象,从而得到铝片与稀盐酸反应是放出热量的。
乙同学不同意甲的结论,理由是 ;
(3)实验结束后,小组同学发现锥形瓶中的液体的量明显多于加入的稀盐酸,请用理化知识解释锥形瓶液体量增多的原因
(1)银白色固体表面有气泡产生,固体不断减少,放热
(2)铝与稀盐酸反应会产生难容的氢气,锥形瓶内气体量增多,沿着导管逸出,也可以产生气泡,不能说明反应放热。
(3)由于反应过程中,放热,导致锥形瓶中部分气体受热逸出,反应结束后,恢复到了室温,锥形瓶中气体比初始时气体少,因此瓶内气压小于外界气压,在大气压作用下,烧杯中的水进入了锥形瓶中。
解析试题分析:活泼金属可以与酸发生反应,所以将稀盐酸加入锥形瓶中与铝接触,可观察到银白色固体表面有气泡产生,固体不断减少,放热;导管口有气泡冒出的现象,可能是由于温度升高引起的,也可能是产生气体引起的,不能说明反应放热;实验结束后,小组同学发现锥形瓶中的液体的量明显多于加入的稀盐酸,由于反应过程中,放热,导致锥形瓶中部分气体受热逸出,反应结束后,恢复到了室温,锥形瓶中气体比初始时气体少,因此瓶内气压小于外界气压,在大气压作用下,烧杯中的水进入了锥形瓶中。
考点:金属的化学性质


 H2SO4浓 =△= CuSO4+SO2↑+2
H2SO4浓 =△= CuSO4+SO2↑+2