��Ŀ����
����Ŀ�������Ѿ�ѧ��ʵ������ȡO2��CO2��������ķ�Ӧԭ������ȡ���ռ�������
��1��������ɳ�ʵ������ȡ���������巴Ӧ�Ĺ�ͬ��������ţ���
A.��Ҫ����
B.����
C.û������μӷ�Ӧ
D.���ɵ�����ֻ��һ��
��2����������ṩ��ʵ��������ҩƷ����ʵ���������Ʊ����о���ʵ����ʵ��������ͼ1��ʾ�����ܺ���Ƥ����δ�������� 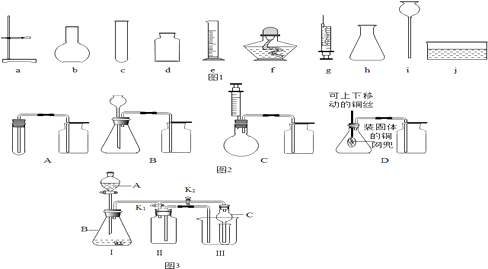
ʵ��ҩƷ��6%˫��ˮ������ʯ��ϡ���ᡢ������ء���������
���Ƚ��о�������д�±�
��ȡ | ��Ӧ��״̬ | ��Ӧ���� | �ռ����������� | |
���� | ���� | ���� | ��ˮ������ | O2��������ˮ�Ҳ���ˮ��Ӧ |
������̼ | �����Һ�� | ���� | CO2�ܶȴ��ڿ����Ҳ��������Ӧ | |
��3����ʵ���о�����ijͬѧѡ��a��c��d��f��j����װ��ȡ���ռ�����װ�ã���ͬѧ��Ӧ����ԭ��Ϊ�����÷��ű���ʽ��ʾ���������Ǹ�ͬѧ���ֲ��������в������� ��
A���ȼ��װ�������ԣ����ҩƷ
B���ȹ̶��Թܣ�����þƾ���
C���Ƚ��������뼯��ƿ��������Թ�
D��ʵ������Ƚ������Ƴ�ˮ�棬��Ϩ��ƾ���
����λͬѧ�����ṩ��ʵ���������ֱ��������ͼ2��ʾ������ȡ���ռ�������̼��װ�ã�
ʵ������ȡ������̼�ķ��ű���ʽΪ �� ��λͬѧ�����װ��������˽������ۣ����п����ռ�����������̼װ�������ܹ�ʹ��Ӧ��ʱֹͣ�ͷ�����װ���� ��
��4������˼С�������ȡ���ռ�װ�õ�ѡ�����ݣ�
����װ�é�����Ӧ���״̬�ͷ�Ӧ����
�ռ�װ�é���������ܶȡ�������ܽ��Ժͻ�ѧ�����е�
��5������չӦ�á���ijͬѧ���������ͼ3��ʾ��ȡ����֤�������ʵ�װ�ã�K1 K2Ϊ���������Ͽ��أ�
�ٵ���K1 �� �ر�K2ʱ���â�װ�ÿ�ֱ�ӽ��е�ʵ����
A������ʯ��ϡ���ᷴӦ�ƶ�����̼
B��п��ϡ���ᷴӦ����������Ӧ������ȣ�
C������غͶ������̻��������
��С��ͬѧ��Ϊ�ڲ��ı��װ�õ�������λ�õ�ǰ���£���װ�ÿ�����˫��ˮ������������������ ��
���𰸡�
��1��CD
��2�������ſ������ռ�
��3��2KMnO4 ![]() K2MnO4+MnO2+O2����BC��CaCO3+2HCl�TCaCl2+CO2��+H2O��A��D
K2MnO4+MnO2+O2����BC��CaCO3+2HCl�TCaCl2+CO2��+H2O��A��D
��4���������������Ӧ
��5��B���ڢ�װ����װ��ˮ���ٽ�����ȡ
���������⣺��1��ͨ��ʵ������ȡO2��CO2��������ķ�Ӧԭ������ȡ���ռ���������������������ȡ�����������̼��ʵ������ȡ������ͬ�ĵط�����Ӧ��Ϊ��Һ�ͣ���Ӧ����Ϊ������ȣ����ɵ������ܶȱȿ������Ҷ����ɵ�����ֻ��һ�֣���2��CO2�ܶȴ��ڿ����Ҳ��������Ӧ�����Կ��������ſ������ռ�����3��ѡ��a��c��d��f��j����װ��ȡ���ռ�����װ�ã�˵�����ü��ȸ�����صķ�����ȡ��������Ӧ�ķ��ű���ʽΪ��2KMnO4 ![]() K2MnO4+MnO2+O2����
K2MnO4+MnO2+O2����
A����ȡ����ʱҪ�ȼ��װ�������ԣ����ҩƷ����ֹװ��©������ȷ��
B������װװ��ʱ���մ����ң����µ��ϵ�˳��Ҫ���ݾƾ��Ƶĸ߶�ȷ���Թܵĸ߶ȣ���B����
C���ȼ����Թܣ�����������������ð���ٿ�ʼ�ռ�����Ϊ��ʼ�����������л���װ���ڵĿ�������C����
D��ʵ������Ƚ������Ƴ�ˮ�棬��Ϩ��ƾ��ƣ���ֹˮ���������Թ�ը�ѣ���ȷ����3��ʵ������ȡ������̼�ô���ʯ��ϡ���ᷴӦ����Ӧ�ķ��ű���ʽΪ��CaCO3+2HCl�TCaCl2+CO2��+H2O��
���Ƕ���Ƶ�װ��������˽������ۣ����п����ռ�����������̼�����װ���ǡ� A�����������Թ���̫�������������嵼�����ܹ�ʹ��Ӧ��ʱֹͣ�ͷ�����װ���� D����ͨ�������ƶ�ͭ˿ʹ��Ӧ������ֹͣ��
����˼С�
���Ͽ�֪���ռ�װ�þ������ܶȡ������ܽ��Ժͻ�ѧ�����е� ���������Ӧ�����жϣ���4������K1 �� �ر�K2ʱ���â�װ�ÿ�ֱ�ӽ��е�ʵ������ȡ������������װ�â��У���������ĵ��ܱȽ϶̣����ֻ���ռ��ܶȱȿ���С�����壬�ʿ�����п��ϡ���ᷴӦ��ȡ�����������Ҫ�ռ������ͱ���ij���ˮ������Ϊ�����ܶȱȿ������ܴӵ��ܽ��������ڢ�װ����װ��ˮ���ٽ�����ȡ��
���Դ��ǣ���1��CD����2�������ſ���������3����2KMnO4 ![]() K2MnO4+MnO2+O2������BC����3��CaCO3+2HCl�TCaCl2+CO2��+H2O��D������˼С��������������Ӧ����5����B������IIװ����װ��ˮ���ٽ�����ȡ��
K2MnO4+MnO2+O2������BC����3��CaCO3+2HCl�TCaCl2+CO2��+H2O��D������˼С��������������Ӧ����5����B������IIװ����װ��ˮ���ٽ�����ȡ��
�����㾫����������д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ����Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪ע�⣺a����ƽ b������ c�����ţ�

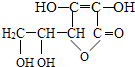
����Ŀ��С��ͬѧ��ѧϰ���й�ά���ص�֪ʶ��������һ�š�ά����C��֪ʶС��Ƭ���������������������д���пո�����ݣ�
��ά����C��֪ʶС��Ƭ | |||
���ӽṹ |
| ��ѧʽ | |
��Է������� | |||
Vc������ | ������ˮ���ڼ��Ȼ���Ի������ױ��������ƻ� | ||
Vc�Ĵ��� | ��ɫ�߲ˣ���ƹϡ����ˣ�/ˮ��������٣� | ||
ʳ�ûƹ���ע�� | |||