题目内容
19.根据下列实验装置填空: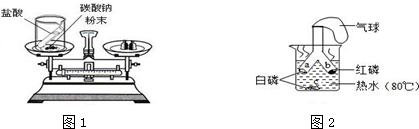
(1)图中反应后天平不平衡,该反应是否符合质量守恒定律?是(填“是”或“否”).
(2)化学反应前后肯定没有变化的是B(填字母序号)
①原子数目 ②分子数目 ③元素种类 ④物质种类 ⑤原子种类 ⑥物质的总质量
A.①④⑥B.①③⑤⑥C.①②⑥D.②③⑤
(3)图2中ac两处(用a、b、c表示)的现象,能证明可燃物须接触空气才能燃烧.
分析 (1)天平不平衡是由于反应后生成了氯化氢气体逸散到空气中,并不是不遵守质量守恒定律.一切化学反应都遵循质量守恒定律;
(2)化学变化是分子分成原子,原子再重新结合成新的分子的过程,据此进行分析解答即可.
(3)根据探究可燃物燃烧的条件的方法来分析.
解答 解:(1)一切化学反应都遵循质量守恒定律,反应后天平不平衡,是因为实验在敞口的容器中进行,生成的氯化氢气体逸出,没有收集称量,所以反应前后质量不相等.
(2)化学反应的实质是分子分成原子,原子再重新组合成新的分子,所以反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有变化,元素的种类、元素的质量、物质的总质量都不变.在此过程中,分子的种类发生了改变,由分子构成的物质的种类也发生了改变;分子数目可能增加也可能减少,也可能前后相等.故化学反应前后一定不变的是①③⑤⑥.
(3)图中出现的现象是:a白磷燃烧,是因为此处的白磷既与氧气接触,温度又达到了白磷的着火点;b处的红磷不燃烧,是因为温度没有达到红磷的着火点;c处的白磷没有燃烧是因为此处的白磷没有接触氧气;
故答案为:(1)是;(2)B;(3)ac.
点评 本题考查的是质量守恒定律的运用,理解微观上质量守恒的原因、注意反应物或生成物中气体易被忽略等是正确解答本题的关键.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
9.根据物质分类知识判断,属于纯净物的是( )
| A. | 洁净的空气 | B. | 干净的汽水 | C. | 干冰 | D. | 矿泉水 |
10.下列固体物质都是白色固体,都能溶于水形成溶液,其中一种溶液外观上与其他三种不同的是( )
| A. | 氯化钠 | B. | 硝酸钾 | C. | 无水硫酸铜 | D. | 纯碱 |
7.2008年奥运会是我们非常关注的,在体育世界中处处充满着化学知识.
(1)“火炬接力”是万世瞩目的,而火炬的燃料是丁烷,请通过下表信息写出丁烷的化学式.
(2)兴奋剂的丑闻时有发生,苯丙胺是其中的一种违禁药物,它的化学式 C9H13N,苯丙胺是由3种元素组成的,它的一个分子中共含有23个原子,一个分子中碳原子与氮原子个数比9:1,其中碳元素和氮元素的质量比为54:7.
(1)“火炬接力”是万世瞩目的,而火炬的燃料是丁烷,请通过下表信息写出丁烷的化学式.
| 物质 | 甲烷 | 乙烷 | 丙烷 | 丁烷 | 戊烷 |
| 化学式 | CH4 | C2H6 | C3H8 | C5H12 |
14.食醋是厨房的一种调味品,其中含有少量醋酸(CH3COOH).下列有关醋酸的说法正确的是( )
| A. | 醋酸是一种氧化物 | |
| B. | 醋酸中碳元素的质量分数为40% | |
| C. | 醋酸是由碳、氢、氧三种原子构成的 | |
| D. | 醋酸中碳、氢、氧三种元素的质量比为2:4:2 |
4.下列物质中含有氧分子的是( )
| A. | 二氧化碳 | B. | 水 | C. | 过氧化氢 | D. | 海水 |
11.密闭容器中有a、b、c、d四种物质,在一定条件下充分反应,测得反应前后个物质的质量如下表所示.下列说法正确的是( )
| 物质 | a | b | c | d |
| 反应前质量/g | 6.40 | 3.20 | 4.00 | 0.50 |
| 反应后质量/g | X | 2.56 | 7.20 | 0.50 |
| A. | d一定是催化剂 | |
| B. | 表中X为2.56 | |
| C. | 该反应为分解反应 | |
| D. | c中元素的种类等于a、b中两种物质中元素的种类之和 |
9.下列化学方程式书写正确的是( )
| A. | CO+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 3O2+4Fe $\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | ||
| C. | 2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑ | D. | NaOH+H2SO4═NaSO4+H2O |