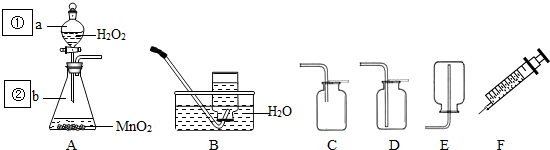
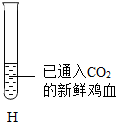
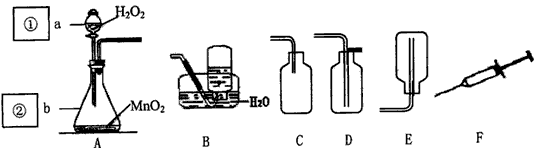
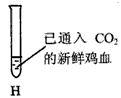
题目内容
实验室制氧气还可以用加热氯酸钾和二氧化锰混合物的方法,其中二氧化锰是催化剂化学方程式是:2KClO3
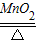 2KCl+3O2↑
2KCl+3O2↑小明同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”,他设计并完成了下表所示的探究实验:
(1)请你帮小明同学填写上表中未填完的空格;
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 各步骤结论 | 总结 | |||
| 实验一 | 将氯酸钾加热至融化,伸入带火星的木条, | 木条复燃 | 氯酸钾受热分解产生氧气,但______. | 二氧化锰是氯酸钾受热分解的催化剂 |
| 实验二 | 加热二氧化锰,伸入带火星的木条, | 木条______ | 加热二氧化锰不能 产生氧气 | |
| 实验三 | ______ | 木条迅速 复 燃 | 二氧化锰能加快氯酸钾 的分解 | |
(3)若要测定实验中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g.依次加热该混合物T1、T2、T3、T4时间后,分别冷却称量剩余固体质量,记录的有关数据见下表:
| 加热时间 | T1 | T2 | T3 | T4 |
| 剩余固体质量 | 4.24g | 4.16g | 4.08g | 4.08g |
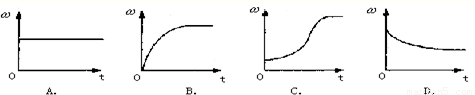
②将氯酸钾和二氧化锰的混合物加热,下列表示二氧化锰在固体混合物中的质量分数ω 随时间t的变化曲线正确的是______
③完全反应后,产生的氧气的总质量为______.
④样品中氯酸钾的质量分数是多少?(请写出计算过程)
【答案】分析:(1)根据实验操作结合已学的运用氯酸钾和二氧化锰的混合物制取氧气时二氧化锰的作用解答
(2)运用实验的分离解答
(3)①运用氯酸钾在二氧化锰做催化剂并加热的条件分解生成氯化钾和氧气解答.
②运用氯酸钾在二氧化锰做催化剂并加热的条件分解生成氯化钾和氧气,反应前后固体总质量减轻,二氧化锰反应前后质量不变解答.
③运用质量守恒定律反应前后固体质量减轻的即生成的氧气解答
④根据氯酸钾制取氧气的化学方程式计算出固体混合物中氯酸钾的质量然后求解.
解答:解:(1)氯酸钾在二氧化锰做催化剂加热的条件下分解产生氯化钾和氧气,二氧化锰做催化剂反应前后质量不变也不会改变反应物和生成物的质量,故(1)答案:放出氧气的速度很慢; 不复燃; 加热氯酸钾和二氧化锰的混合物
(2)显然这两个实验是对比实验,故(2)答案:对比
(3)①氯酸钾在二氧化锰做催化剂并加热的条件分解生成氯化钾和氧气,氧气是气体,其余的都是固体,故①答案:KCl MnO2
②二氧化锰在这一反应中做催化剂所以固体二氧化锰的质量始终不变,但氯酸钾随着反应的进行会不断分解生成氯化钾和氧气所以固体质量不断减轻,因此固体中二氧化锰的质量分数会不断增大,但到氯酸钾全部分解固体质量就不会改变二氧化锰的质量分数也不会改变.所以选C.
③反应前后固体质量减轻的既是产生的氧气6g-4.08g=1.92g,
④设:固体中氯酸钾的质量为x
2KClO3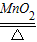 2KCl+3O2↑
2KCl+3O2↑
245 96
x 1.92g
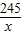 =
=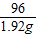
x=4.9g
样品中氯酸钾的质量分数是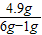 ×100%=98%
×100%=98%
答:样品中氯酸钾的质量分数为98%
点评:化学是一门以实验为基础的科学,实验可以帮助我们获取很多新知识,验证一些现象与结论.因此,学习化学时,不要错过每一个实验,更不要轻易放过实验中的每一个现象.
(2)运用实验的分离解答
(3)①运用氯酸钾在二氧化锰做催化剂并加热的条件分解生成氯化钾和氧气解答.
②运用氯酸钾在二氧化锰做催化剂并加热的条件分解生成氯化钾和氧气,反应前后固体总质量减轻,二氧化锰反应前后质量不变解答.
③运用质量守恒定律反应前后固体质量减轻的即生成的氧气解答
④根据氯酸钾制取氧气的化学方程式计算出固体混合物中氯酸钾的质量然后求解.
解答:解:(1)氯酸钾在二氧化锰做催化剂加热的条件下分解产生氯化钾和氧气,二氧化锰做催化剂反应前后质量不变也不会改变反应物和生成物的质量,故(1)答案:放出氧气的速度很慢; 不复燃; 加热氯酸钾和二氧化锰的混合物
(2)显然这两个实验是对比实验,故(2)答案:对比
(3)①氯酸钾在二氧化锰做催化剂并加热的条件分解生成氯化钾和氧气,氧气是气体,其余的都是固体,故①答案:KCl MnO2
②二氧化锰在这一反应中做催化剂所以固体二氧化锰的质量始终不变,但氯酸钾随着反应的进行会不断分解生成氯化钾和氧气所以固体质量不断减轻,因此固体中二氧化锰的质量分数会不断增大,但到氯酸钾全部分解固体质量就不会改变二氧化锰的质量分数也不会改变.所以选C.
③反应前后固体质量减轻的既是产生的氧气6g-4.08g=1.92g,
④设:固体中氯酸钾的质量为x
2KClO3
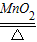 2KCl+3O2↑
2KCl+3O2↑245 96
x 1.92g
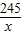 =
=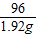
x=4.9g
样品中氯酸钾的质量分数是
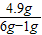 ×100%=98%
×100%=98%答:样品中氯酸钾的质量分数为98%
点评:化学是一门以实验为基础的科学,实验可以帮助我们获取很多新知识,验证一些现象与结论.因此,学习化学时,不要错过每一个实验,更不要轻易放过实验中的每一个现象.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
实验室制氧气还可以用加热氯酸钾和二氧化锰混合物的方法,其中二氧化锰是催化剂化学方程式是:
2KClO3 2KCl+3O2↑
2KCl+3O2↑
小明同学欲通过实验证明“二氧化锰是氯酸钾受热分解的催化剂”,他设计并完成了下表所示的探究实验:
(1)请你帮小明同学填写上表中未填完的空格;
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 各步骤结论 | 总结 | |||
| 实验一 | 将氯酸钾加热至融化,伸入带火星的木条, | 木条复燃 | 氯酸钾受热分解产生氧气,但______. | 二氧化锰是氯酸钾受热分解的催化剂 |
| 实验二 | 加热二氧化锰,伸入带火星的木条, | 木条______ | 加热二氧化锰不能 产生氧气 | |
| 实验三 | ______ | 木条迅速 复 燃 | 二氧化锰能加快氯酸钾 的分解 | |
(3)若要测定实验中氯酸钾样品的纯度,取一定质量的该样品与1g二氧化锰混合,其总质量为6g.依次加热该混合物T1、T2、T3、T4时间后,分别冷却称量剩余固体质量,记录的有关数据见下表:
| 加热时间 | T1 | T2 | T3 | T4 |
| 剩余固体质量 | 4.24g | 4.16g | 4.08g | 4.08g |
②将氯酸钾和二氧化锰的混合物加热,下列表示二氧化锰在固体混合物中的质量分数ω 随时间t的变化曲线正确的是______
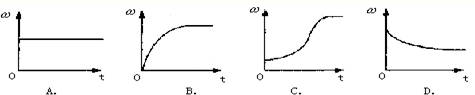
③完全反应后,产生的氧气的总质量为______.
④样品中氯酸钾的质量分数是多少?(请写出计算过程)