题目内容
【题目】2020年新型冠状病毒引起的肺炎在我国部分地区造成的疫情在全国人民的共同努力下得到了较好的控制。为防传染,很多部门用过氧乙酸对环境消毒,已知过氧乙酸的化学式为C2H4O3。下列有关过氧乙酸的说法正确的是()
A.属于无机物
B.氧元素质量分数最大
C.相对分子质量为78
D.是由2个碳原子、4个氢原子和3个氧原子构成
【答案】B
【解析】
某元素质量分数=![]() ×100%,各元素质量之比=
×100%,各元素质量之比=![]() 之比,各元素质量分数之比=
之比,各元素质量分数之比=![]() ×100%之比,故各元素质量之比=各元素质量分数之比;
×100%之比,故各元素质量之比=各元素质量分数之比;
A、由过氧乙酸的化学式可知,过氧乙酸是一种含碳元素的化合物,属于有机物,故选项错误;
B、过氧乙酸中碳、氢、氧元素的质量比为(12×2):(1×4):(16×3)=6:1:12,可见其中氧元素的质量分数最大,故选项正确;
C、过氧乙酸的相对分子质量为12×2+1×4+16×3=76,故选项错误;
D、过氧乙酸是由分子构成的,每个过氧乙酸分子是由2个碳原子、4个氢原子和3个氧原子构成的,故选项错误。故选B。

【题目】某实验小组选择“铜和硫酸反应的探究”的课题开展探究,下表是他们分别用相同质量的铜粉和足量硫酸反应的几组实验数据:
实验编号 | 硫酸的质量分数/% | 温度/℃ | 铜粉消失的时间/s |
① | 98 | 120 | 400 |
② | 98 | 200 | 200 |
③ | 80 | 120 | 500 |
④ | 80 | 200 | 280 |
⑤ | 70 | 200 | 不消失 |
⑥ | 40 | 200 | 不消失 |
(1)实验①、②表明:该反应快慢与__________有关,其关系是_______________;能表明硫酸浓度对反应快慢有影响的实验编号组合是_____________。
(2)如果把实验①中硫酸的质量分数改为85%,请你推出铜粉消失时间(用t表示)的取值范围_______。
(3)从上表来看,能与铜粉发生反应的硫酸溶液最低浓度a%的范围是_________(取整数)。
(4)影响金属和酸化学反应速度的因素除了上述因素以外还可能有____________________。
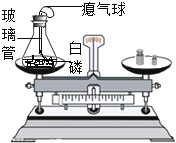
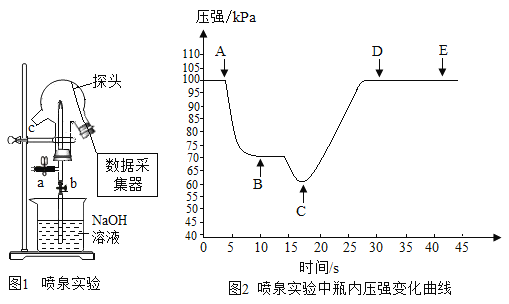
(拓展延伸)已知浓硫酸与铜粉加热时产生刺激性气体氧化物,同时溶液变蓝。如图是利用压强传感器测定浓硫酸与铜粉加热产生气体与NaOH溶液产生喷泉实验过程及压强变化曲线图。
(5)请写出铜粉与浓硫酸加热生成刺激性气体和溶液变蓝的化学方程式_________________。
(6)实验过程:三颈瓶内装有收集满的气体,采集数据,将吸有NaOH溶液的胶头滴管塞紧颈口c,挤尽胶头滴管液体,然后打开阀门b,烧杯内的NaOH溶液喷到三颈瓶内形成喷泉,则曲线AB段下降的原因是_____________;CD段上升的原因是___________________。
【题目】请从1或2两题中任选1个作答。
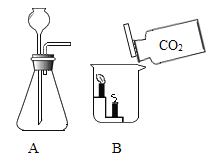
O2的实验室制取与性质 | CO2的实验室制取与性质 |
(1)A中加热高锰酸钾,发生反应的化学方程式为___________。 (2)B中可观察到的现象是__________。 |
(1)A中向大理石中加入稀盐酸,发生反应的化学方程式为__________。 (2)B中可观察到的现象是__________。 |