题目内容
(2011?綦江县)某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2.小青同学设计了以下实验方案来除去可溶性杂质.
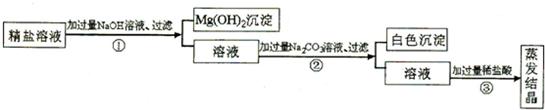
(1)步骤①的化学方程式为
(2)步骤②中得到的白色沉淀是
(3)步骤③中加稀盐酸是为了除去溶液中的
A.CaCl2 B.MgCl2 C.NaOH D.Na2C03.

(1)步骤①的化学方程式为
2NaOH+MgCl2═2NaCl+Mg(OH)2↓
2NaOH+MgCl2═2NaCl+Mg(OH)2↓
.(2)步骤②中得到的白色沉淀是
CaCO3
CaCO3
(填化学式).(3)步骤③中加稀盐酸是为了除去溶液中的
C D
C D
.A.CaCl2 B.MgCl2 C.NaOH D.Na2C03.
分析:除钙离子用碳酸根,除镁离子用氢氧根,因为加入的试剂都是过量的,所以后加的试剂要把先加的试剂所带入的杂质除掉,加入过量的稀盐酸,这样可以除去多余的碳酸根离子和氢氧根离子.
解答:解:本实验的过程为①加过量NaOH溶液,与MgCl2发生反应,生成Mg(OH)2沉淀和氯化钠;
②加过量Na2CO3溶液,与CaCl2发生反应,生成CaCO3沉淀和氯化钠,过滤,滤出前面生成的沉淀;
③加适量盐酸,与①中过量NaOH溶液和②中过量Na2CO3溶液发生反应,生成氯化钠、水和二氧化碳气体;蒸发、结晶,得到精盐.
故答案为:
(1)2NaOH+MgCl2═2NaCl+Mg(OH)2↓;
(2)CaCO3;
(3)C D.
②加过量Na2CO3溶液,与CaCl2发生反应,生成CaCO3沉淀和氯化钠,过滤,滤出前面生成的沉淀;
③加适量盐酸,与①中过量NaOH溶液和②中过量Na2CO3溶液发生反应,生成氯化钠、水和二氧化碳气体;蒸发、结晶,得到精盐.
故答案为:
(1)2NaOH+MgCl2═2NaCl+Mg(OH)2↓;
(2)CaCO3;
(3)C D.
点评:通过离子间的反应把离子转化为沉淀和气体除去,但要注意加入试剂的量,最后不能带入新的杂质.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
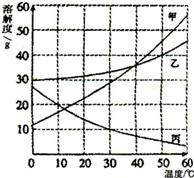 (2011?綦江县)甲、乙、丙三种固体物质的溶解度曲线如图所示.
(2011?綦江县)甲、乙、丙三种固体物质的溶解度曲线如图所示.