��Ŀ����
����Ŀ���Ķ�������ն��ģ�Ȼ��ش�����
������ͨ��״�����ǵ���ɫ�������ȳ�ζ�����塣�������ȶ���һ�����ȼ���ת����O2�����ų��������ȡ�O2������������O2ǿ�öࡣ����O2ͨ���������������������ŵ������£��ӳ���������������O2�к���Լ3%��O2��
�����ڵ��渽���Ĵ������к������٣��������Լ25km����һ����ȼ����ij����dz�����������̫�������еĴ��������ߣ�ʹ�����ϵ��������������ߵ��˺�������һ�������ı����㡣
�����ٷɻ��ų������е�CO��CO2��NO�����壬���õ������ʹ�õ�����������������ȶԳ������кܴ���ƻ����ã���ʹ�������γɿն����Ӷ�ʹ��������������䵽������棬����Ƥ�����ķ����ʴ�����ӡ��粻��ȡ��ʩ������������롣
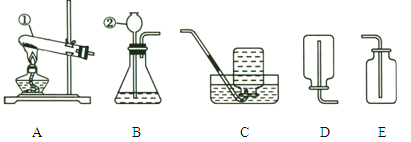
��1���������ǵ�ľ�����뵽ʢ�г����ļ���ƿ�У��ɿ���_____������ԭ��_____
��2��Ӧ����_____���������㡣
��3��SO2��O3�ȼ���Ѹ��������SO3��SO3��ˮ��Ӧ�������ᣬ���dz�ȥ������SO2�����뷽����SO2��O2��Ӧ�����ֱ���ʽΪ_____����ת��ɳ����Ĺ����з�����_____����������������ѧ�����仯��
��4������������������_____��
���𰸡�ľ����ȼ�� �����ֽܷ��������� ʹ�������䣨�������������ŷţ� ��������+����![]() �������� ��ѧ�� ����ɫ�������ȳ�ζ������
�������� ��ѧ�� ����ɫ�������ȳ�ζ������
��������
��1������������������ǿ���������ֽ�����������Խ������ǵ�ľ�����뵽ʢ��O3�ļ���ƿ�У����Կ���ľ����ȼ������
��2���������֪��Ӧ��ȡ����һ����̼��������̼��һ��������������ŷţ���ʹ������������������ķ��������������㣻
��3��SO2��O3�ȼ���Ѹ��������SO3����Ӧ�����ֱ���ʽΪ����������+����![]() �������������ͳ������ڲ�ͬ���ʣ���������ת��ɳ����Ĺ����з����˻�ѧ�仯��
�������������ͳ������ڲ�ͬ���ʣ���������ת��ɳ����Ĺ����з����˻�ѧ�仯��
��4��O3�����������ǵ���ɫ�������ȳ�ζ�����塣

 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д� �������ϵ�д�
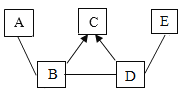
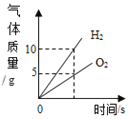
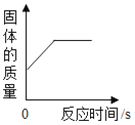
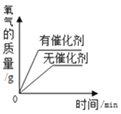
�������ϵ�д�����Ŀ������4��ͼ���У�����ȷ��ӳ�仯��ϵ���ǣ�������
|
|
|
|
A����ˮͨ����һ��ʱ�� | B��þ�ڿ����м��� | C������һ�������ĸ�����ع��� | D����������ȫ��ͬ�Ĺ���������Һ�ֱ���ȡ���� |
A. A B. B C. C D. D
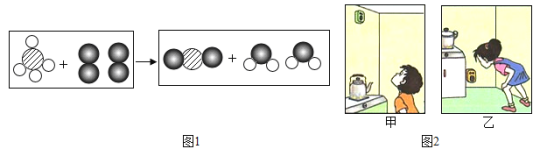
����Ŀ��ij�о�С������ͼ��ʾװ�ã�̽���ܷ���þ��������ײⶨ����������������
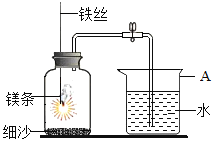
��������룩
����1�����Դ��棬��Ϊþ����������Ӧ���������
����2�����ܴ��棬��Ϊþ�����ܻ�������е������ɷַ�����Ӧ
������ʵ�飩
���� | ʵ����� | ʵ������ |
�� | ��װ��װ�ú�ֹˮ�У����漯��ƿ��һ��ʱ����ɿ��� | �ձ��е��ܿ�������ð�������ֺ��ձ��е���ĩ����һ��Һ�� |
�� | �ر�ֹˮ�У���ȼþ����Ѹ�����뼯��ƿ�У��������� | þ��ȼ�գ��ų������ȣ�����ҫ�۰⣬���ɴ������̣�ʣ�����Ϊ��ɫ��״�ﻹ�����ż���������ɫ�Ĺ��� |
�� | ��ȴ�����£���ֹˮ�� | �ձ���ˮ�ӵ��ܽ��뼯��ƿ�У����ԼΪ����ƿ����� |
����������ۣ�
��1��������ʵ��Ŀ����_____��
��2��������У��ر�ֹˮ�е�Ŀ����_____��
��3������ʵ�������е�_____��дһ�����ɣ������Ʋ����2������
�٣�����̽�������������ϵ�֪����þ��Mg3N2��Ϊ����ɫ�Ĺ��壬����С�����þ�������ܻ�������е�_____������Ӧ��
�ڣ����ʵ�飩�����ʵ�鷽��֤���Լ��IJ���_____��
�ۣ�ʵ����ۣ�þ���뵪����Ӧ�Ļ�ѧ����ʽΪ��_____��
�ܣ���˼�����ۣ�ͨ������̽��������ȼ����ʲô�µ���ʶ��_____��