题目内容
将25g甲物质与5g乙物质发生反应,所得混合物中含有10g甲、11g丙,还有另一种物质丁.若甲、乙、丙、丁的相对分子质量分别为30、20、44、18,化学式分别表示为A、B、C、D,则下列化学方程式中正确的是( )A.A+B═C+D
B.A+2B═2C+D
C.2A+B═2C+D
D.2A+B═C+2D
【答案】分析:根据质量守恒定律及化学方程式的意义可以知道,物质的相对分子质量的和的比值和实际质量的比值相等,所以可以据此来判断反应中各物质的化学计量数.
解答:解:根据反应的特点可以知道,反应前后质量减少的为反应物,而质量增加的为生成物,所以可以判断反应中消耗了甲的质量为:25g-10g=15g,乙物质完全被消耗,即为5g,即反应物为甲和乙,而丙和丁为生成物,其质量为11g,根据质量守恒定律可以知道生成了丁的质量为:15g+5g-11g=9g,设甲的化学计量数为a,乙物质的化学计量数为b,则可以得出比例式为: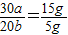 ,所以
,所以 =
= ,设生成物中丙的化学计量数为c,丁的化学计量数为d,则可得比例式为:
,设生成物中丙的化学计量数为c,丁的化学计量数为d,则可得比例式为: =
= 所以可以得出
所以可以得出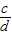 =
= ,所以可以写出该反应的化学方程式为:2A+B═C+2D,分析所给的选项可以知道选项D是正确的.
,所以可以写出该反应的化学方程式为:2A+B═C+2D,分析所给的选项可以知道选项D是正确的.
故选D.
点评:解这类题时不能把加入的各物质简单地理解为反应物,应考虑过量问题,然后运用质量守恒定律和化学方程式可表示各物质之间质量比解题.
解答:解:根据反应的特点可以知道,反应前后质量减少的为反应物,而质量增加的为生成物,所以可以判断反应中消耗了甲的质量为:25g-10g=15g,乙物质完全被消耗,即为5g,即反应物为甲和乙,而丙和丁为生成物,其质量为11g,根据质量守恒定律可以知道生成了丁的质量为:15g+5g-11g=9g,设甲的化学计量数为a,乙物质的化学计量数为b,则可以得出比例式为:
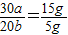 ,所以
,所以 =
= ,设生成物中丙的化学计量数为c,丁的化学计量数为d,则可得比例式为:
,设生成物中丙的化学计量数为c,丁的化学计量数为d,则可得比例式为: =
= 所以可以得出
所以可以得出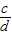 =
= ,所以可以写出该反应的化学方程式为:2A+B═C+2D,分析所给的选项可以知道选项D是正确的.
,所以可以写出该反应的化学方程式为:2A+B═C+2D,分析所给的选项可以知道选项D是正确的.故选D.
点评:解这类题时不能把加入的各物质简单地理解为反应物,应考虑过量问题,然后运用质量守恒定律和化学方程式可表示各物质之间质量比解题.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目