题目内容
某工厂产生的废渣主要成分是含钙的化合物(杂质为Fe2O3)。用该废渣制取CaCl2晶体(CaCl2•xH2O)并进行组成测定,其制取的流程如图1所示:
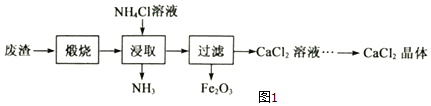
已知:NH4Cl溶液显酸性,且浓度越高酸性越强
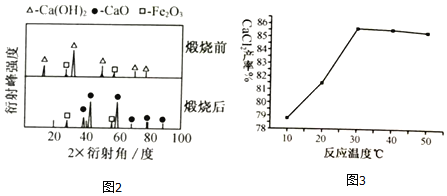
(1)XRD图谱可用于判断某固态物质是否存在。图2为煅烧前后废渣的XRD图谱。写出煅烧时发生的化学反应方程式_____。
(2)浸取时需连续搅拌,其目的是_____;生成的NH3能使湿润的红色石蕊试纸变_____色。
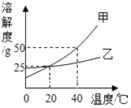
(3)在其它条件相同的情况下,CaCl2的产率随浸取温度的变化如图3所示。则宜选择的浸取温度为_____0C左右。
(4)若使用过量浓度较高的NH4Cl溶液,则所得CaCl2溶液中会含有NH4Cl、_____(填化学式)等杂质。
(5)测定晶体(CaCl2•xH2O)的组成:
a 称取14.7000g CaCl2晶体于锥形瓶内,加入适量蒸馏水。使其全部溶解。
b 再向其中加入足量的Na2CO3溶液,静置。
c _____、_____、干燥、称量,得到10.0000g固体。
①通过计算,确定x的值为_____。
②判断步骤b中沉淀完全的方法是:_____,则说明已沉淀完全;若沉淀不完全,则测得的x值比实际值_____(填“偏大”、“偏小”或“不变”)。
练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
下表中,有关量的变化图像与其对应叙述相符的是
A | B | C | D |
|
|
|
|
浓硫酸敞口放置一段时间 | 向一定质量的氧化铁粉末中加入稀盐酸 | 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn粉 | 向一定质量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D