题目内容
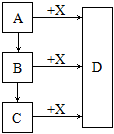
对反应:X+H2SO4=BaSO4↓+2Y,下面分析正确的是
| A.Y中可能含有氢元素 | B.Y可能是HCl |
| C.X一定是BaCl2 | D.X和Y的相对分子质量之差一定为l35 |
B
试题分析:质量守恒定律可知:化学反应前后元素的种类、原子个数和种类、质量不变;A.反应物中含有氢元素,硫酸钡中不含有氢元素,Y中一定含有氢元素,故A说法错误;B.由质量守恒定律,若反应中Y是HCl时,X为BaCl2,符合题意,所以Y可能是HCl,故B正确;C.当X是Ba(OH)2时,氢氧化钡与硫酸的反应符合X+H2SO4═BaSO4↓+2Y,故X不一定是BaCl2.故C说法错误;
D、根据质量守恒定律可知化学反应前后各物质的相对分子质量之和相等,硫酸钡与硫酸的相对分子质量之差为135,因为Y的系数是2,X和Y的相对分子质量之差不是135.故D错误.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目