题目内容
【题目】电镀厂的废水中含有Cu(NO3)2和AgNO3,为处理水体污染并回收金属,某兴趣小组的同学进行下列实验(如下图所示):向含有Cu(NO3)2和AgNO3的废水中加入一定量的铁粉,过滤,得固体A和滤液B,向固体A中滴加稀盐酸,无明显现象,小组同学对所得滤液B的成分进行探究。
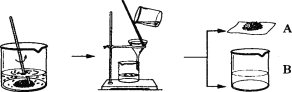
【提出问题】过滤后所得滤液B中含有哪些成分?
【猜想与假设】
甲同学:滤液B中只含有Fe(NO3)2;
乙同学:滤液B中只含有Fe(NO3)2和AgNO3两种溶质;
丙同学:滤液B中只含有AgNO3和Cu(NO3)2两种溶质;
【表达与交流】写出甲同学猜想的理由:(1) ;
【反思与评价】请对乙同学的猜想做出评价:(2) ;
【实验探究】取滤液少许于试管中,向滤液中插入一根铜丝,看到铜丝表面有固体生成,则滤液B中溶质的化学式应该是(3) ;
【归纳总结】通过上述实验探究可知,在分析金属与盐溶液反应后的溶质成分时,需考虑的方面有(4) (至少答两方面)。
【答案】(1)加入的铁粉和溶液中的硝酸铜、硝酸银恰好完全反应,生成可溶的硝酸亚铁。
(2)错。铁粉先与硝酸银反应,后与硝酸铜反应,若有硝酸银,则硝酸铜一定剩余。
(3)Fe (NO3)2、Cu(NO3)2、AgNO3
(4)反应的先后顺序;可溶性生成物;剩余的可溶性反应物。(任意两点,合理即可)
【解析】
试题分析:(1)向固体A中滴加稀盐酸,无明显现象,说明A中无Fe,有关的化学方程式是:Fe+2AgNO3= Fe(NO3)2+2Ag,Fe+ Cu(NO3)2= Fe(NO3)2+ Cu,当加入的铁粉和溶液中的硝酸铜、硝酸银恰好完全反应,生成可溶的硝酸亚铁。(2) Fe与Ag活动性差别较大,故Fe先与AgNO3溶液反应,当AgNO3溶液反应完以后,Fe才与Cu(NO3)2溶液反应,如果AgNO3溶液有剩余,则Fe没与Cu(NO3)2溶液反应,故乙同学的猜想是错误的。(3)取滤液少许于试管中,向滤液中插入一根铜丝,看到铜丝表面有固体生成,则滤液中含有AgNO3溶液,当有AgNO3溶液时,Cu(NO3)2溶液没有与Fe反应,故滤液中有没反应的Cu(NO3)2、生成的Fe(NO3)2、剩余的AgNO3 (4)通过上述实验探究可知,在分析金属与盐溶液反应后的溶质成分时,需考虑的方面有反应的先后顺序、可溶性生成物、剩余的可溶性反应物。

 名校课堂系列答案
名校课堂系列答案