题目内容
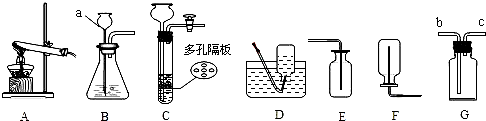
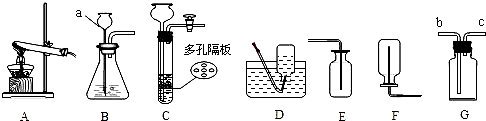
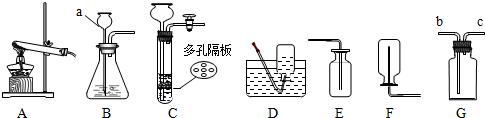
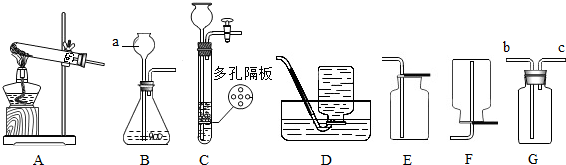
请结合下列实验室制取气体的常用装置,回答有关问题.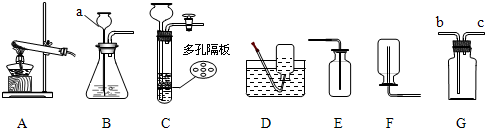
(1)写出图中标有字母的仪器名称:a______.
(2)若用氯酸钾和二氧化锰的混合物制取氧气,应选用的发生装置是______ (填“A、B或C”),在加入药品前,应首先______,反应的化学方程式是______.
(3)某同学欲用G装置代替D装置,用排水法收集一种难溶性气体,该同学使用G装置的方法是______.
(4)实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是______.
(5)在实验室还可选用B装置用H2O2溶液和MnO2来制取O2.取一瓶久置后的过氧化氢溶液,取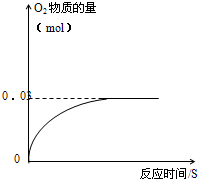 出102g,加入适量的二氧化锰,充分反应后生成氧气的物质的量与反应时间的关系如图所示:
出102g,加入适量的二氧化锰,充分反应后生成氧气的物质的量与反应时间的关系如图所示:
求:
①完全反应后生成氧气质量______g.
②该102g过氧化氢溶液中所含H2O2的物质的量是多少?(列式计算)
③计算该溶液中溶质的质量分数______.
解:(1)仪器名称为长颈漏斗
(2)氯酸钾二氧化锰是固体,反应条件是加热,故发生装置A,实验开始前要先检查装置气密性,化学方程式为:
2KClO3 2KCl+3O2↑
2KCl+3O2↑
(3)G装置内装满水,气体从短管进入,将水从长管排出.
(4)固体放在有孔塑料板上,固液接触发生反应,分离反应停止,因此可通过开关止水夹随时控制气体的发生.
(5)根据图象可知完全反应后生成氧气的物质的量为0.03mol,所以质量为32×0.03=0.96g;根据氧气的物质的量可求出过氧化氢溶液中过氧化氢的物质的量.从而求出过氧化氢的质量及质量分数.
故答案为:(1)长颈漏斗
(2)A 检查气密性 2KClO3 2KCl+3O2↑
2KCl+3O2↑
(3)先将G装置装满水,气体从c端通入
(4)可以随时控制气体的发生
(5)①0.96g
②2H2O2 2H2O+O2↑
2H2O+O2↑
2 1
X 0.03 mol

X=0.06 mol
质量为0.06mol×34g/mol=2.04g
③所以溶质的质量分数等于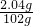 ×100%=2%
×100%=2%
分析:根据反应条件和反应物状态选择发生装置,排水法装置内先装满水,用气体将水排出来;要控制反应随时发生需固液完全分离;根据物质的量与相对分子质量之间的关系进行转化求解.
点评:本题考查制取气体的装置的选择 优缺点的判断及根据化学方程式的计算,题目难度不大.
(2)氯酸钾二氧化锰是固体,反应条件是加热,故发生装置A,实验开始前要先检查装置气密性,化学方程式为:
2KClO3
 2KCl+3O2↑
2KCl+3O2↑(3)G装置内装满水,气体从短管进入,将水从长管排出.
(4)固体放在有孔塑料板上,固液接触发生反应,分离反应停止,因此可通过开关止水夹随时控制气体的发生.
(5)根据图象可知完全反应后生成氧气的物质的量为0.03mol,所以质量为32×0.03=0.96g;根据氧气的物质的量可求出过氧化氢溶液中过氧化氢的物质的量.从而求出过氧化氢的质量及质量分数.
故答案为:(1)长颈漏斗
(2)A 检查气密性 2KClO3
 2KCl+3O2↑
2KCl+3O2↑(3)先将G装置装满水,气体从c端通入
(4)可以随时控制气体的发生
(5)①0.96g
②2H2O2
 2H2O+O2↑
2H2O+O2↑ 2 1
X 0.03 mol

X=0.06 mol
质量为0.06mol×34g/mol=2.04g
③所以溶质的质量分数等于
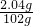 ×100%=2%
×100%=2%分析:根据反应条件和反应物状态选择发生装置,排水法装置内先装满水,用气体将水排出来;要控制反应随时发生需固液完全分离;根据物质的量与相对分子质量之间的关系进行转化求解.
点评:本题考查制取气体的装置的选择 优缺点的判断及根据化学方程式的计算,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目

 出102g,加入适量的二氧化锰,充分反应后生成氧气的物质的量与反应时间的关系如图所示:
出102g,加入适量的二氧化锰,充分反应后生成氧气的物质的量与反应时间的关系如图所示: