题目内容
某不纯的铁5.6g与足量的稀硫酸充分反应,生成0.21g氢气,则铁中混有的金属可能是( )
| A.Zn | B.Cu | C.Mg | D.Ag |
试题分析:铜、银不能和稀硫酸反应;解:设5.6g铁与足量的稀硫酸充分反应生成氢气的质量为X, Fe+H2SO4═FeSO4+H2↑56 25.6g X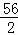 =
=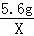 X=0.2g;解:设5.6g锌与足量的稀硫酸充分反应生成氢气的质量为Y, Zn+H2SO4═ZnSO4+H2↑65 25.6g Y
X=0.2g;解:设5.6g锌与足量的稀硫酸充分反应生成氢气的质量为Y, Zn+H2SO4═ZnSO4+H2↑65 25.6g Y 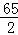 =
=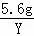 Y=0.17g,解:设5.6g镁与足量的稀硫酸充分反应生成氢气的质量为Z, Mg+H2SO4═MgSO4+H2↑24 25.6g Z
Y=0.17g,解:设5.6g镁与足量的稀硫酸充分反应生成氢气的质量为Z, Mg+H2SO4═MgSO4+H2↑24 25.6g Z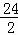 =
=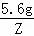 Z=0.47g,由以上计算可知,当5.6g纯铁与足量稀硫酸反应时能够生成0.2g氢气,当5.6g纯锌与足量稀硫酸反应时能够生成0.17g氢气,当5.6g纯镁与足量稀硫酸反应时能够生成0.47g氢气,由此可知,不纯的铁5.6g中,如果含有锌,则生成的氢气小于0.2g,如果含有镁,则生成的氢气大于0.2g,不纯的铁5.6g与足量的稀硫酸充分反应,生成0.21g氢气,则铁中混有的金属可能是镁.故选:C.
Z=0.47g,由以上计算可知,当5.6g纯铁与足量稀硫酸反应时能够生成0.2g氢气,当5.6g纯锌与足量稀硫酸反应时能够生成0.17g氢气,当5.6g纯镁与足量稀硫酸反应时能够生成0.47g氢气,由此可知,不纯的铁5.6g中,如果含有锌,则生成的氢气小于0.2g,如果含有镁,则生成的氢气大于0.2g,不纯的铁5.6g与足量的稀硫酸充分反应,生成0.21g氢气,则铁中混有的金属可能是镁.故选:C.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目