题目内容
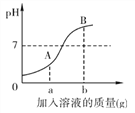
【题目】如图是稀硫酸和NaOH溶液反应的pH变化曲线,以下说法正确的是
A. A点溶液中滴入紫色石蕊试液变蓝
B. B点之前滴加BaCl2溶液不会产生白色沉淀
C. 表示的是将NaOH溶液滴入稀硫酸中
D. 该反应的化学方程式为:H2SO4+NaOH=Na2SO4+H2O
【答案】C
【解析】A、A点时溶液的pH小于7,溶液显酸性,滴入紫色石蕊试液变红,故选项说法错误;B、A-B两点间的任意溶液中均含有生成的硫酸钠,硫酸钠与氯化钡溶液反应生成硫酸钡白色沉淀,加BaCl2溶液都会产生硫酸钡白色沉淀,故选项说法错误;C、由图象可知,pH值的变化是从小于7逐渐的减小到大于7,可知原溶液显酸性,然后不断的加入碱性溶液,使pH增大,说明是把NaOH溶液滴加到稀硫酸中,故选项说法正确;D、该反应的化学方程式为:H2SO4+2NaOH=Na2SO4+2H2O,故选项说法错误。故选C。

练习册系列答案
相关题目