题目内容
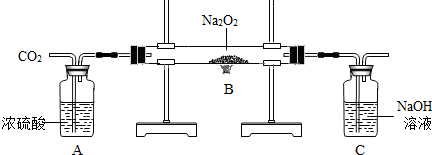
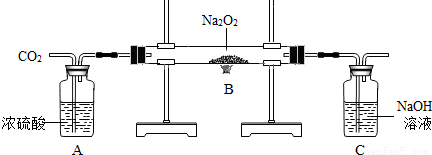
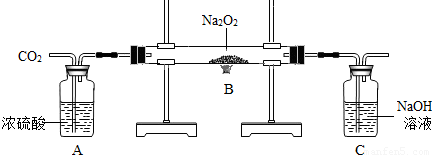
实验小组的同学为探讨过氧化钠(Na2O2)与二氧化碳的反应,用如图所示的装置进行实验.通入CO2气体,将带火星的木条放在C的导管口中,木条复燃.请回答下列问题: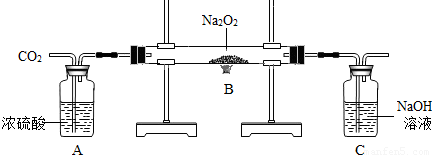
(1)根据木条复燃的情况,推测Na2O2与CO2发生的反应,写出化学方程式______.
(2)请设计一种实验方案验证该反应的另一种产物______
______.
【答案】分析:将二氧化碳通过浓硫酸,能除去水,再与过氧化钠反应,能生成使带火星木条复燃的气体,说明生成氧气,根据质量守恒定律,化学反应前后,元素的种类不变,生成的另一种物质必含碳钠元素,可能含氧元素,根据学过的物质可能为碳酸钠.检验碳酸钠就是涉及到的碳酸盐的检验,采用加酸化气的方法.
解答:(1)根据质量守恒定律,化学反应前后,元素的种类不变,生成的另一种物质必含碳、钠元素,可能含氧元素,根据学过的物质推测为碳酸钠,所以本题答案为:2Na2O2+2CO2=2Na2CO3+O2;
(2)证明碳酸钠的存在就是涉及到碳酸盐的检验,可以采用向所得固体中加入酸液,观察是否生成能使澄清石灰水变浑浊的气体,所以本题答案为:取白色固体,加稀盐酸,产生能使澄清石灰水变混浊的气体,证明推测正确的;反之,推论不正确.
点评:要推测化学反应中生成物质的化学式,需依据质量守恒定律,而要检验是否生成碳酸钠,就是涉及碳酸盐的检验,采用加酸观察能否产生使澄清石灰水变浑浊的气体.
解答:(1)根据质量守恒定律,化学反应前后,元素的种类不变,生成的另一种物质必含碳、钠元素,可能含氧元素,根据学过的物质推测为碳酸钠,所以本题答案为:2Na2O2+2CO2=2Na2CO3+O2;
(2)证明碳酸钠的存在就是涉及到碳酸盐的检验,可以采用向所得固体中加入酸液,观察是否生成能使澄清石灰水变浑浊的气体,所以本题答案为:取白色固体,加稀盐酸,产生能使澄清石灰水变混浊的气体,证明推测正确的;反之,推论不正确.
点评:要推测化学反应中生成物质的化学式,需依据质量守恒定律,而要检验是否生成碳酸钠,就是涉及碳酸盐的检验,采用加酸观察能否产生使澄清石灰水变浑浊的气体.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 30、实验小组的同学为探讨过氧化钠(Na2O2)与二氧化碳的反应,用如图所示的装置进行实验.通入CO2气体,将带火星的木条放在C的导管口中,木条复燃.
30、实验小组的同学为探讨过氧化钠(Na2O2)与二氧化碳的反应,用如图所示的装置进行实验.通入CO2气体,将带火星的木条放在C的导管口中,木条复燃.