题目内容
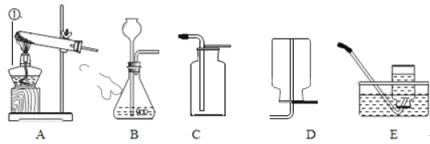
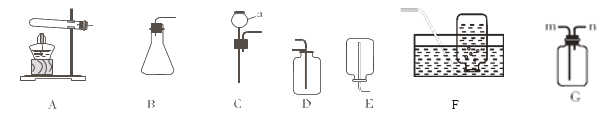
【题目】某同学设计了如图所示的装置,用于实验室制取CO2,并对它的部分性质进行探究,按要求回答问题。
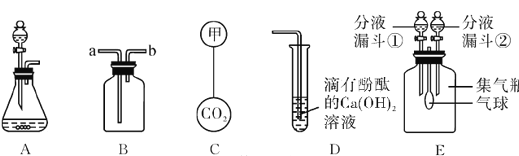
(1)请写出A装置中一种玻璃仪器的名称____
(2)A装置用于制取CO2,反应的化学方程式为____
(3)用B装置收集CO2,气体应从_____ (选填“a”或“b”)端通入。
(4)若要C中的两个气球悬浮在空气中,则气体甲可能是_____ (填序号)。
A.氢气 B.氧气 C.空气
(5)往D试管中通入CO2,当出现_____溶质恰好完全沉淀。
(6)E装置的集气瓶中充满CO2,打开分液漏斗①,滴入少量NaOH浓溶液,气球明显胀大,写出发生反应的化学方程式____若要气球恢复原状,应关闭分液漏斗②,滴入____(填化学式,忽略滴入液体体积)。
【答案】分液漏斗/锥形瓶 CaCO3+2HCl=CaCl2+H2O+CO2↑ a A 溶液红色褪去时 2NaOH+H2O=Na2CO3+H2O HCl
【解析】
(1)A装置中的玻璃仪器有分液漏斗、锥形瓶;
(2)用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)用B装置收集CO2,气体应从长管a进入,因为氧气的密度比空气大;
(4)若要C中的两个气球悬浮在空气中,则气体甲可能是氢气,因为氢气的密度比空气小;(5)往D试管中通入CO2,当出现溶液红色刚好消失现象,表示石灰水中的溶质恰好完全沉淀;
(6)二氧化碳和氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;若要气球恢复原状,应关闭分液漏斗①,打开分液漏斗②,滴入稀盐酸。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目