题目内容
【题目】工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4,为了测定铁红中铁的质量分数,兴趣小组的同学称取10.0g铁红样品进行如下实验,请你参与过程分析。
(资料)1.草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:![]()
2.浓硫酸具有吸水性,氢氧化钠溶液可以吸收CO2。
3.碱石灰的主要成分是CaO和NaOH,可以吸收水与CO2。
(问题讨论)用下图所示装置实行实验:
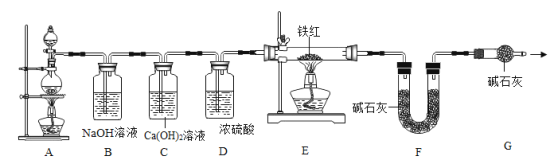
(1)实验前应先_____。
(2)C装置的作用是_____。
(3)对E装置加热前和停止加热后,都要通入过量的CO,其作用分别是:①加热前_____;②停止加热后把反应生成的二氧化碳全部排入F装置中。
(4)写出E装置中所发生反应的一个化学方程式_____。
(数据分析与计算)
(5)充分反应后称得F装置增重6.6g,则此铁红中铁的质量分数是_____。
(实验评价)
(6)本实验中如果缺少D装置(不考虑其它因素),则测得样品中铁的质量分数会_____(填“偏小”、“不变”或“偏大”)。
(7)请指出实验装置的一个明显缺陷_____。
【答案】进行装置气密的检查 检验B装置是否将二氧化碳气体吸收完全 将装置内的空气排尽,防止发生危险 Fe2O3+3CO![]() 2Fe+3CO2 76.0% 偏低 缺少尾气处理装置
2Fe+3CO2 76.0% 偏低 缺少尾气处理装置
【解析】
(1)实验前应先:进行装置气密的检查,确保实验成功;
(2)C装置的作用是:检验B装置是否将二氧化碳气体吸收完全,不影响后续实验的顺利进行;
(3)对E装置加热前和停止加热后,都要通入过量的CO,其作用分别是:一氧化碳具有可燃性,①加热前通入一氧化碳是将装置内的空气排尽,防止发生危险;②停止加热后把反应生成的二氧化碳全部排入F装置中。
(4)E装置中一氧化碳在高温条件下与氧化铁反应产生铁和二氧化碳所的化学方程式:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(5)充分反应后称得F装置增重6.6g,6.6g是二氧化碳的质量,由质量守恒定律可知,铁红中氧元素质量为=6.6g![]() ,则此铁红中铁的质量分数=
,则此铁红中铁的质量分数=![]() .
.
(6)本实验中如果缺少干燥剂D装置,则F装置增重变大,因为吸收了水蒸气,则样品中的氧元素质量偏大,测得样品中铁的质量分数会偏小。
(7)一氧化碳有毒,不能直接排放到空气中,实验装置的一个明显缺陷:缺少尾气处理装置。

 名校课堂系列答案
名校课堂系列答案【题目】某同学设计以下实验探究氧化铜能否作为过氧化氢分解制取氧气的催化剂,以及影响化学反应速率的因素。
实验序号 | H2O2溶液浓度/% | H2O2溶液体积/mL | 温度/℃ | 催化剂种类及用量/g | 氧气体积/mL | 收集氧气所用时间/s |
① | 5 | 10 | 20 | 无 | 100 | - |
② | 5 | 10 | 20 | 二氧化锰1g | 100 | 15 |
③ | 5 | 10 | 40 | 二氧化锰1g | 100 | 8 |
④ | 10 | 10 | 20 | 二氧化锰1g | 100 | 5 |
⑤ | 5 | 10 | 20 | 氧化铜1g | 100 | 22 |
(1)通过实验____和____对比,说明过氧化氢分解的速率与温度有关。
(2)通过实验____和____对比,说明过氧化氢分解的速率与浓度有关。
(3)通过实验____和____对比,说明氧化铜粉末能加快过氧化氢分解速率。
(4)想要证明氧化铜是该反应的催化剂,还需要验证其在反应前后____和____没有发生改变。
(5)①写出氧化铜催化过氧化氢分解的文字表达式:__________。
②根据以上实验得出的结论,在下图中画出有、无氧化铜时过氧化氢分解产生氧气的质量与反应时间的关系图____________。