题目内容
小明同学在公共场所的围墙上看到一则化肥广告(如图)。回校后,他想利用所学化学知识判断该广告是否是虚假广告,请你与小明同学一起完成下列计算:

(1)硝酸铵的化学式量为__________;
(2)硝酸铵中氮元素:氢元素:氧元素质量比为__________;
(3)硝酸铵中氮元素的质量分数是多少?(写出计算过程,计算结果精确到1%)小明同学判断这则广告是虚假广告,请解释小明同学判断的依据______________。
(4)小明认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现氮元素质量分数仅为28%,则该产品中硝酸铵的质量分数为__________。(注明:该小问属于附加题,可选做。)

(1)硝酸铵的化学式量为__________;
(2)硝酸铵中氮元素:氢元素:氧元素质量比为__________;
(3)硝酸铵中氮元素的质量分数是多少?(写出计算过程,计算结果精确到1%)小明同学判断这则广告是虚假广告,请解释小明同学判断的依据______________。
(4)小明认为此广告会坑害农民,向有关部门反映,技术监督局对该产品取样分析,发现氮元素质量分数仅为28%,则该产品中硝酸铵的质量分数为__________。(注明:该小问属于附加题,可选做。)
(1)80
(2)7:1:12
(3)35%
硝酸铵最高含氮量为35%,而广告上硝酸铵的含量氮为38%,所以是虚假广告。
(4)80%。
(2)7:1:12
(3)35%
硝酸铵最高含氮量为35%,而广告上硝酸铵的含量氮为38%,所以是虚假广告。
(4)80%。
试题分析:解:(1)硝酸铵的化学式量为14×2+1×4+16×3=80;
(2)硝酸铵中氮元素:氢元素:氧元素质量比为14×2:1×4:16×3=;7:1:12。
(3)硝酸铵中氮元素的质量分数是=
 ×100%
×100%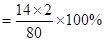 =35%。
=35%。硝酸铵最高含氮量为35%,而广告上硝酸铵的含量氮为38%,所以是该广告是虚假广告。
(4)设取Ag样品检验,样品中硝酸铵的质量分数为x%,则:
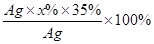 =28%
=28%x%=80%
即该化肥中含硝酸铵的质量分数为80%。
点评:根据化学式可以计算化合物的相对分子质量、元素质量分数、元素质量比等。
化合物的相对分子质量等于化合物中各元素相对原子质量的总和;
化合物中各元素的质量比等于各元素相对原子质量与原子个数乘积的比。
某元素的质量分数=
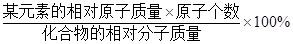 。
。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 12CO2↑+10H2O↑+6X↑+O2↑
12CO2↑+10H2O↑+6X↑+O2↑