题目内容
【题目】如图是a、b、c三种物质的溶解度曲线: 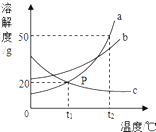
①P点的意义是;
②t2℃时,将50g a物质放入50g水中充分溶解,得到a的溶液的质量为g(a物质不含结晶水);
③t2℃时,a、b、c三种物质的溶解度由大到小的顺序为:;将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是;
④t2℃时,将c的饱和溶液变为不饱和溶液,可采用的方法.
【答案】在t1℃时,a、c的溶解度相等;75;a>b>c;b>a>c;增加溶剂或减少溶质
【解析】解:(1)由溶解度曲线可知:P点的意义是:在t1℃时,a、c的溶解度相等;所以答案是:在t1℃时,a、c的溶解度相等;(2)t2℃时,a的溶解度是50g,将50ga物质放入50g水中充分溶解,得到a的溶液的质量=25g+50g=75g;所以答案是:75;(3)t2℃时,a、b、c三种物质的溶解度由大到小的顺序为:a>b>c;将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是b>a>c,因为a析出固体比b多,c由饱和变为不饱和溶液,还是最小;所以答案是:a>b>c;b>a>c;(4)t2℃时,将c的饱和溶液变为不饱和溶液,可采用增加溶剂或减少溶质的方法,所以答案是:增加溶剂或减少溶质;
【考点精析】通过灵活运用饱和溶液和不饱和溶液相互转变的方法和固体溶解度曲线及其作用,掌握饱和和不饱和的转变方法:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低②最可靠的方法是:加溶质、蒸发溶剂;1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和)即可以解答此题.