题目内容
【题目】取23.44g质量分数为16%的Ba(NO3)2溶液于烧杯中,逐渐加入K2CO3溶液.实验过程中,生成BaCO3沉淀的质量与加入K2CO3溶液的质量关系如图所示. 
(1)当加入30.5g K2CO3溶液时,生成沉淀的总质量为g.
(2)计算A点溶液中溶质的质量分数.
【答案】
(1)3.94
(2)解:A点时碳酸钾与硝酸钡恰好完全反应,所得溶液是硝酸钾溶液.设A点时溶液中溶质的质量为x.
K2CO3+Ba(NO3)2═ | BaCO3↓+ | 2KNO3 |
197 | 202 | |
3.94g | x |
![]() =
= ![]()
解得x=4.04g
所以A点时溶液中溶质的质量分数为 ![]() ×100%=8.08%
×100%=8.08%
答:A点时溶液中溶质的质量分数为8.08%
【解析】解:(1)根据图象可直接看出,当加入30.5g K2CO3溶液时,生成沉淀的总质量为3.94g,所以答案是:3.94g;
【考点精析】本题主要考查了根据化学反应方程式的计算的相关知识点,需要掌握各物质间质量比=系数×相对分子质量之比才能正确解答此题.

练习册系列答案
相关题目
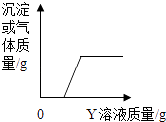
【题目】在下表①﹣④组的X溶液中,滴加Y溶液至过量,生成沉淀或气体的质量与加入Y溶液的质量关系符合图的是
X溶液 | Y溶液 | |
① | CuCl2溶液和HCl溶液 | NaOH溶液 |
② | Na2SO4溶液和H2SO4溶液 | BaCl2溶液 |
③ | NaCl溶液和HCl溶液 | NaHCO3溶液 |
④ | Na2CO3溶液和NaOH溶液 | H2SO4溶液 |
( )
A.①③
B.②③
C.①④
D.②④