题目内容
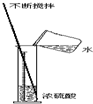 某同学按如图所示配制实验所需的稀硫酸,请指出错误所在
某同学按如图所示配制实验所需的稀硫酸,请指出错误所在错误①
将水加入到浓硫酸中
将水加入到浓硫酸中
.错误②在量筒中稀释
在量筒中稀释
.分析:浓硫酸的稀释:“酸入水,沿器壁,慢慢倒,不断搅.”.另外,量筒不能不能作反应容器或者用于配置溶液.
解答:解:稀释生浓硫酸时,应把浓硫酸缓缓注入盛有水的烧杯中,并用玻璃棒不断搅拌,量筒只用来量取液体,不能用来配制溶液,
故填:将水加入到浓硫酸中;在量筒中稀释.
故填:将水加入到浓硫酸中;在量筒中稀释.
点评:该题主要考查了稀释浓硫酸的方法,可以依据浓硫酸的性质和仪器的使用进行.

练习册系列答案
相关题目

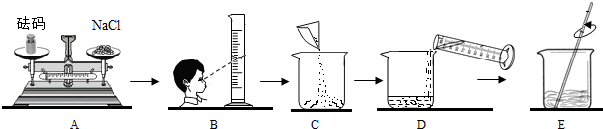
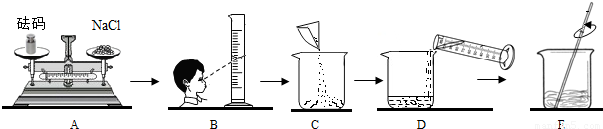
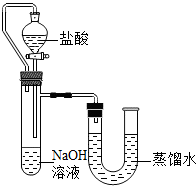 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其证明与某盐酸发生了中和反应.