��Ŀ����
����Ŀ��ʹ����ͼ��ʾװ����ȡ������ 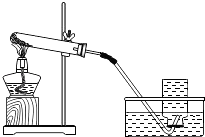
��1��д�����ȸ�������������Ļ�ѧ����ʽ����
��2��ָ����ͼװ����һ�����ԵIJ���֮������
��3�������ռ���ɺ���䴿������ƫ�ͣ�ԭ������ǣ�������ĸ���ɶ�ѡ����
A.��������л����˶�������
B.�ռ�ǰ������ƿ��δע��ˮ
C.�ռ�����ƿ����������ˮ
D.δ��������������ð��ʱ�Ϳ�ʼ�ռ�
��4�����о���������ȡ���������ʼ��䷴Ӧ�������Ĺ����У�ijͬѧ������±���ʾϵ��ʵ�飺
��� | ʵ�� | �ܷ��������� |
A | ���ȸ������ | �� |
B | ���ȶ������� | ���� |
C | �����Ȼ��� | ���� |
D | ����ˮ | ���� |
E | ���ˮ | �� |
�ٸ���ʵ��A��B��C�����Եó��Ľ����ǣ���һ�������£���
�ڸ���ʵ��D��E�����Եó��Ľ����ǣ���Ӱ�������ܷ�Ӧ������������Ҫ���أ�
��5����10g������ؼ���һ��ʱ��Ƶ�ʣ����������Ϊ9.36g���Լ��㣺 �ٲ���������������
��ʣ�������ص�������
���𰸡�
��1��2KMnO4 ![]() K2MnO4+MnO2+O2��
K2MnO4+MnO2+O2��
��2���Թܿ�δ��һ����
��3��BD
��4�����������������ȡ���������ʣ���Ӧ����
��5���⣺���������غ㶨�ɿ�֪��������������Ϊ10g��9.36g=0.64g��
����μӷ�Ӧ��KMnO4����Ϊx��
2KMnO4 | O2�� |
316 | 32 |
x | 0.64g |
![]() =
= ![]() �����x=6.32g��
�����x=6.32g��
���ʣ��KMnO4����Ϊ10g��6.32g=3.68g
��6.32g��10g
��KMnO4δ��ȫ��Ӧ
ʣ���KMnO4����=10g��6.32g=3.68g
�𣺢ٲ�������������Ϊ0.64g����ʣ�����и�����ص�������3.68g
���������⣺��1��������ؼ�����������ء��������̺��������ʴ𰸣�2KMnO4 ![]() K2MnO4+MnO2+O2������2�����ȸ������������ʱ�Թܿ�Ҫ��һ�������Է�������ط�ĩ���뵼�ܣ����Դ��ǣ��Թܿ�δ��һ��������3��A����������л����˶������̣������������Ĵ���û��Ӱ�죬�ʴ��� B���ռ�ǰ������ƿ��δע��ˮ���ͻ��������ݣ�ʹ�ռ�����������ƫ�ͣ�����ȷ��
K2MnO4+MnO2+O2������2�����ȸ������������ʱ�Թܿ�Ҫ��һ�������Է�������ط�ĩ���뵼�ܣ����Դ��ǣ��Թܿ�δ��һ��������3��A����������л����˶������̣������������Ĵ���û��Ӱ�죬�ʴ��� B���ռ�ǰ������ƿ��δע��ˮ���ͻ��������ݣ�ʹ�ռ�����������ƫ�ͣ�����ȷ��
C���ռ�����ƿ����������ˮ��ֻ�ᵼ������û���ռ����������������Ĵ���û��Ӱ�죬�ʴ���
D��δ��������������ð��ʱ�Ϳ�ʼ�ռ������װ���ڵ����������ռ�������ƿ�ڣ�ʹ�ռ�����������ƫ�ͣ�����ȷ��
��ѡBD����4���ٸ���ʵ��A��B��C��֪һ�������£�ֻ�и�������ֽܷ������������˸��������������ȡ���������ʣ����Դ��ǣ����������������ȡ���������ʣ���ͬ�Ƿ�Ӧ��ˮ�����Ȳ��ܲ�������������ܲ����������ɴ˿�֪��Ӧ������Ӱ�������ܷ�Ӧ������������Ҫ���أ����Դ��ǣ���Ӧ������
�����㾫����������Ĺؼ�����������������ȡװ�õ����֪ʶ�����շ���װ�ã��̹̼����͡���Һ�������ͣ��Լ����������ռ����������⣬�˽��ռ�װ�ã��������ʵ��ܶȡ��ܽ��ԣ���ˮ���ռ�ʱ�������ݾ�������ð��ʱ���ռ����տ�ʼ�ų������Թ��еĿ����������ſ������ռ�����ʱ�������쵽����ƿ�ײ���

 ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д� Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д�