题目内容
(8分)某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如下图所示),大大提高了资源利用率,减少了环境污染。请填写:
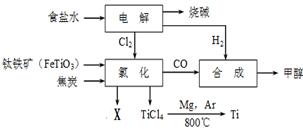
(1)氯碱厂用电解饱和食盐水的方法制取烧碱,同时得到氯气和氢气。写出其化学方程式: 。
(2)钛酸亚铁(FeTiO3)中钛元素的化合价是 。钛冶炼厂氯化车间的氯化过程发生如下反应:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X的化学式为 ,其名称为 。
(3)试写出TiCl4与Mg反应生成金属Ti的化学方程式 ,该反应属于 反应。上述反应需在氩气环境中进行,理由是 。
(4)同温同压下,任何气体之间的体积比就是它们的分子数之比。在一定条件下用H2和CO化合生成甲醇(化学方程式是2H2 + CO = CH3OH),则合成甲醇时,H2和CO两种气体的体积比应为 。

(1)氯碱厂用电解饱和食盐水的方法制取烧碱,同时得到氯气和氢气。写出其化学方程式: 。
(2)钛酸亚铁(FeTiO3)中钛元素的化合价是 。钛冶炼厂氯化车间的氯化过程发生如下反应:2FeTiO3+6C+7Cl2=2X+2TiCl4+6CO,则X的化学式为 ,其名称为 。
(3)试写出TiCl4与Mg反应生成金属Ti的化学方程式 ,该反应属于 反应。上述反应需在氩气环境中进行,理由是 。
(4)同温同压下,任何气体之间的体积比就是它们的分子数之比。在一定条件下用H2和CO化合生成甲醇(化学方程式是2H2 + CO = CH3OH),则合成甲醇时,H2和CO两种气体的体积比应为 。
(1) 2NaCl+2H2O 通电 2NaOH+Cl2↑+H2↑ (2) +4 FeCl3 氯化铁 (3) TiCl4+2Mg 800℃, Ti+2MgCl2 置换 作保护气
(4) 2∶1
(4) 2∶1
(1)由题意可知,该反应的反应物为氯化钠与水,生成物为氢氧化钠、氢气和氯气,反应条件为通电,故可书写此化学方程式
(2)根据化合物中正负化合价的代数和为0,质量守恒定律解答
(3) TiCl4+2Mg 800℃, Ti+2MgCl2可知,反应物中镁属于单质,四氯化钛属于化合物,(4)根据生成物中钛属于单质,氯化镁属于化合物,该反应属于置换反应.进行解答
同温同压下,任何气体之间的体积比就是它们的分子数之比
(2)根据化合物中正负化合价的代数和为0,质量守恒定律解答
(3) TiCl4+2Mg 800℃, Ti+2MgCl2可知,反应物中镁属于单质,四氯化钛属于化合物,(4)根据生成物中钛属于单质,氯化镁属于化合物,该反应属于置换反应.进行解答
同温同压下,任何气体之间的体积比就是它们的分子数之比

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
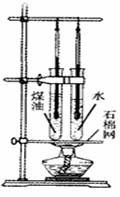
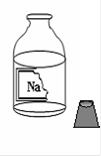




 现象
现象