题目内容
【题目】化学用语是学习化学的重要工具。
(1)写出下列微粒的化学符号:
锌原子______;氮气分子______;二氧化硫分子______;氢氧根离子______。
(2)用下列字母序号填空:a.干冰 b.金刚石 c.液氮 d.不锈钢
①______可用于切割玻璃;②______可用于医疗手术;
③______用于制造医疗器械;④______可用于人工降雨。
(3)写出下列反应的化学方程式:
①红磷与氧气反应______;②氢氧化钠与硫酸铜溶液反应____;
③用双氧水制取氧气______;④硝酸铵受热分解生成N2O气体和水____。
【答案】 Zn N2 SO2 OH— b c d a ![]()
![]()
![]() 【答题空10】
【答题空10】![]()
![]()
![]()
![]()
![]()
![]()
![]()
【解析】(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字。所以锌原子可表示为:Zn;根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此氮气分子可表示为:N2;二氧化硫分子表示为:SO2;由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。氢氧根离子可表示为:OH—;(2)①金刚石是硬度最大的物质,可用来裁割玻璃;②液氮可制作冷冻剂,可用于医疗手术;③不锈钢不易生锈,耐腐蚀,可用于制造医疗器械;④干冰升华吸热,可用于人工降雨;(3)①红磷与氧气反应生成五氧化二磷固体,化学反应方程式为: ![]()
![]()
![]() ;②氢氧化钠与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,化学反应方程式为:
;②氢氧化钠与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,化学反应方程式为: ![]() ;③用双氧水制取氧气,化学方程式为:
;③用双氧水制取氧气,化学方程式为: ![]()
![]()
![]() ;④硝酸铵受热分解生成N2O气体和水,化学方程式为:
;④硝酸铵受热分解生成N2O气体和水,化学方程式为: ![]()
![]()
![]() 。
。

 名校课堂系列答案
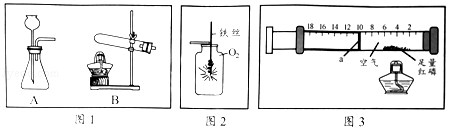
名校课堂系列答案【题目】某校化学兴趣小组利用下列仪器在实验室进行制取O2的相关实验探究,请回答下列问题。

(1)甲小组用MnO2、KClO3两种药品制取干燥的O2,需选用的仪器组合是_____________,反应结束后回收MnO2固体,操作依次是冷却至室温、___________、过滤、____________、烘干。
(2)乙小组探究Fe2O3能否作为H2O2分解的催化剂。实验时间为30s(H2O2过量),其他可能影响实验的因素均保持不变,相关数据如下:
实验 序号 | 10%的H2O2 溶液(mL) | 溶液中加入 物质(g) | 收集到气体的 体积(mL) |
1 | 100 | 无 | a |
2 | 100 | Fe2O3 0.5g | b |
3 | 100 | MnO2 0.5g | c |
通过比较_______和_______(填“a”“b”“c”)的大小,可证明Fe2O3在实验中起催化作用,写出该反应的化学方程式_______________________________________________。其次需补做实验,验证反应前后Fe2O3的化学性质不变和验证__________________________________。
(3)丙小组探究MnO2的用量对H2O2分解速率的影响。每次均用30mL 10%的H2O2溶液,使用不同质量的MnO2作催化剂,测定每次收集到500mL O2所用的时间。结果如图(其他实验条件相同):
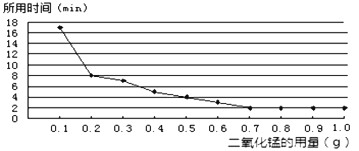
由图可知,MnO2的用量对H2O2分解速率影响的规律是:
①_____________________________________________________;
②MnO2的用量超出一定范围后,其用量再增大,反应速率不再继续加快。