题目内容
 红色粉末是由Cu、Fe2O3二种固体组成,某同学为测定其成分做了如下实验:称取该粉末5.0g装入硬质玻璃管中,
红色粉末是由Cu、Fe2O3二种固体组成,某同学为测定其成分做了如下实验:称取该粉末5.0g装入硬质玻璃管中,
| 反应前 | 反应后 | |
| Ⅰ组 | 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
| Ⅱ组 | 洗气瓶和所盛溶液的总质量为180.0g | 洗气瓶和瓶中物质的总质量为183.1g |
(2)不选择Ⅱ组实验数据的原因是______.
方法一:设固体粉末中氧化铁的质量为x
3CO+Fe2O3
 2Fe+3CO2;固体质量减少
2Fe+3CO2;固体质量减少160 112 48
x 1.2g

x=4g
方法二:红色粉末中只有氧化铁中含有氧元素,故可根据氧元素的质量求出氧化铁的质量为:
 =4g
=4g则红色粉末中Fe2O3的质量分数为:
 ×100%=80%
×100%=80%答:红色粉末中Fe2O3的质量分数为80%
(2)因为不能证明生成的二氧化碳完全与澄清石灰水反应,故不选择第Ⅱ组数据;
故答案为:(1)红色粉末中Fe2O3的质量分数为80%;(2)第Ⅱ组数据,不能证明二氧化碳完全反应;
分析:根据第Ⅰ组实验数据计算出氧元素的质量,根据氧元素全部来自与氧化铁,故可求出氧化铁的质量,然后求出氧化铁在固体粉末中的质量分数;
第二组数据中因不能证明二氧化碳完全与澄清石灰水反应,故不能利用质量的增加求出氧化铁的质量.
点评:本题考查了根据化学方程式的计算以及质量分数的计算,考查注重基础.

实验一:用干燥纯净的一氧化碳还原氧化铁
实验装置如下图:

其中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:
 。请回答下列问题:
。请回答下列问题:(1)B装置中发生反应的化学方程式是 .
(2)C装置无明显现象,C装置的作用是 。
D装置中浓硫酸的作用是 。
(3)E装置中的实验现象是 。
(4)F装置的作用是 、 。
实验二:铝粉和氧化铁粉末反应(铝热反应)
实验装置如下图:

图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中。
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨。请写出该反应的化学方程式 。该反应中单质铝与一氧化碳有相似的 (填“氧化”或“还原”)性。
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情。
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究。
【实验方案】
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热。 向冷却后的固体中加入足量的稀盐酸。 | 黑色粉末变成 色 固体部分溶解,有气泡产生,水溶液呈无色。 | Zn和CuO能发生置换反应。 |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热。 向冷却后的固体中加入足量的稀盐酸。 | 发生爆炸,黑色粉末变成红色。 固体部分溶解,有气泡产生,水溶液呈 色。 | |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热。 | 粉末无变化 | Cu、Fe2O3不能反应。 |
【实验总结】金属与金属氧化物在高温条件下有些能反应,有些不能反应。
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与 的反应相似。
(2011年江苏无锡,35题)钢铁是使用最多的金属材料。在今年的化学活动周中,某校兴趣小组的同学在老师指导下做了二个有关铁的实验。
实验一:用干燥纯净的一氧化碳还原氧化铁
实验装置如下图:
其中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是: 。请回答下列问题:
。请回答下列问题:
(1)B装置中发生反应的化学方程式是 .
(2)C装置无明显现象,C装置的作用是 。
D装置中浓硫酸的作用是 。
(3)E装置中的实验现象是 。
(4)F装置的作用是 、 。
实验二:铝粉和氧化铁粉末反应(铝热反应)
实验装置如下图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中。
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨。请写出该反应的化学方程式 。该反应中单质铝与一氧化碳有相似的 (填“氧化”或“还原”)性。
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情。
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究。
【实验方案】
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热。 向冷却后的固体中加入足量的稀盐酸。 | 黑色粉末变成 色 固体部分溶解,有气泡产生,水溶液呈无色。 | Zn和CuO能发生置换反应。 |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热。 向冷却后的固体中加入足量的稀盐酸。 | 发生爆炸,黑色粉末变成红色。 固体部分溶解,有气泡产生,水溶液呈 色。 | |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热。 | 粉末无变化 | Cu、Fe2O3不能反应。 |
【实验总结】金属与金属氧化物在高温条件下有些能反应,有些不能反应。
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与 的反应相似。
实验一:用干燥纯净的一氧化碳还原氧化铁
实验装置如下图:

其中A是实验室用草酸(H2C2O4)和浓硫酸加热制取一氧化碳的气体发生装置,反应的化学方程式是:H2C2O4
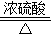 H2O+CO2↑+CO↑.请回答下列问题:
H2O+CO2↑+CO↑.请回答下列问题:(1)B装置中发生反应的化学方程式是 .
(2)C装置无明显现象,C装置的作用是 .
D装置中浓硫酸的作用是 .
(3)E装置中的实验现象是 .
(4)F装置的作用是 、 .
实验二:铝粉和氧化铁粉末反应(铝热反应)
实验装置如下图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式 .该反应中单质铝与一氧化碳有相似的 (填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
提出问题:任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
实验方案:
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成 色 固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈 色. | |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |
反思拓展:金属与金属氧化物在高温条件下反应的规律和金属与 的反应相似.



