题目内容
【题目】(1)用化学用语填空。
①3个铁原子________;②2个镁离子________;
③n个臭氧分子________;④在硫酸根离子中硫元素的化合价为+6价________。
(2)某元素R在人体内能调节体液平衡,缺乏该元素会造成心率不齐,过量则会使人恶心腹泻。该元素的原子结构示意图为 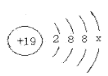 。请回答:
。请回答:
①x的值为________;
②该元素形成氧化物的化学式为________。
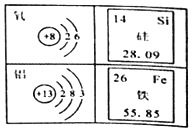
③该元素的化学性质与下面________元素的化学性质相似(填序号)
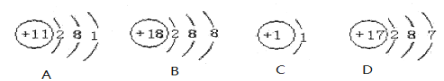
【答案】3Fe ![]() nO3
nO3 ![]() 1 R2O(或K2O) A
1 R2O(或K2O) A
【解析】
由原子中,质子数=核外电子数,可以计算出x的数值;由该元素的原子得失电子的情况,可以判断该元素的化合价,进而可以确定形成氧化物的化学式;根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,决定元素的化学性质的是最外层电子数,据此分析判断即可。
(1)
①3个铁原子就是在铁元素符号的前面加上数字3,故填:3Fe;
②表示多个离子时就在其离子符号前加上相应的数字,故2个镁离子可表示为:2Mg2+;
③n臭氧分子就是在臭氧化学式的前面加上字母n,故填:nO3;
④在元素符号正上方的数字表示元素的化合价,正负号在前,数字在后,硫酸根离子中硫元素的化合价为+6价,表示为![]() ;
;
(2)
①在原子中,质子数=核外电子数, x的值为19-2-8-8=1;
②根据元素的原子结构示意图可知质子数为19,是钾元素,最外层电子数是1,易失去电子显+1价,氧元素显-2价,根据化合物中各元素化合价代数和为零可知,该元素形成氧化物的化学式为K2O;
③元素的化学性质跟它的原子的最外层电子数目关系非常密切,即最外层电子数相同的元素化学性质相似,由结构示意图可知A与C的最外层电子数为1,但C是氢元素,为非金属元素,与该元素化学性质不同,所以该元素的化学性质与A的化学性质相似。