题目内容
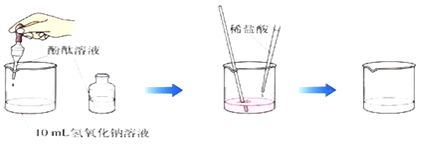
化学兴趣小组在学习了酸、碱、盐的化学性质后,进行了如下图所示的实验:

(1)写出甲实验中盐酸和氢氧化钙反应的化学方程式 ,当观察到甲中出现 的现象时,证明二者发生了反应;
(2)乙实验中观察到有白色沉淀产生;
(3)实验结束后,同学们将甲、乙两个实验的废液倒入同一个干净的废液缸中,最终观察到废液呈浑浊状,原因是其中含 (填化学式);
【提出问题】将上述废液过滤,滤液中含哪些物质呢?
【交流讨论】
①你认为滤液中一定含指示剂、水和 (填化学式);
②若滤液呈无色,则一定呈中性,不可能为呈酸性,原因是 ;
③若该滤液呈红色,则溶液呈碱性,能使溶液呈碱性的物质是什么?
第一组同学认为:只有氢氧化钙
第二组同学认为:只有氢氧化钠
第三组同学认为:是碳酸钠和氢氧化钠
你认为还可能是 (写一种猜想)。
【实验验证】

(1)写出甲实验中盐酸和氢氧化钙反应的化学方程式 ,当观察到甲中出现 的现象时,证明二者发生了反应;
(2)乙实验中观察到有白色沉淀产生;
(3)实验结束后,同学们将甲、乙两个实验的废液倒入同一个干净的废液缸中,最终观察到废液呈浑浊状,原因是其中含 (填化学式);
【提出问题】将上述废液过滤,滤液中含哪些物质呢?
【交流讨论】
①你认为滤液中一定含指示剂、水和 (填化学式);
②若滤液呈无色,则一定呈中性,不可能为呈酸性,原因是 ;
③若该滤液呈红色,则溶液呈碱性,能使溶液呈碱性的物质是什么?
第一组同学认为:只有氢氧化钙
第二组同学认为:只有氢氧化钠
第三组同学认为:是碳酸钠和氢氧化钠
你认为还可能是 (写一种猜想)。
【实验验证】
| 实验内容 | 现象 | 结论 |
| 取少量滤液于试管中,加入过量Ca(NO3)2溶液,静置 | | 第三组同学的猜想正确 |
(1)Ca(OH)2+2HCl==CaCl2+2H2O , 红色逐渐褪去 ;
(3) CaCO3 ;
① NaCl ; ②废液中含碳酸钙,不可能还含酸 ;
③ 碳酸钠(氢氧化钠和氢氧化钙) 。
(3) CaCO3 ;
① NaCl ; ②废液中含碳酸钙,不可能还含酸 ;
③ 碳酸钠(氢氧化钠和氢氧化钙) 。
| 实验内容 | 现象 | 结论 |
| 取少量滤液于试管中,加入过量Ca(NO3)2溶液,静置 | 产生白色沉淀,溶液仍为红色 | 第三组同学的猜想正确 |
分析:由题目的信息可知:甲实验中盐酸和氢氧化钙反应生成氯化钙和水,配平即可;当观察到甲中出现红色逐渐褪去时,证明恰好完全反应.碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠;最终观察到废液呈浑浊状,原因是其中含白色沉淀碳酸钙;废液过滤,滤液中一定含有氯化钠;若滤液呈无色,则一定呈中性,不可能为呈酸性,原因是废液中含碳酸钙,不可能还含酸;若该滤液呈红色,则溶液呈碱性,能使溶液呈碱性的物质可能是:氢氧化钙;氢氧化钠;碳酸钠;或碳酸钠和氢氧化钠;或氢氧化钠和氢氧化钙.如果产生白色沉淀,溶液仍为红色,那么猜想三正确.
解答:解:(1)甲实验中盐酸和氢氧化钙反应生成氯化钙和水,配平即可;当观察到甲中出现红色逐渐褪去时,证明恰好完全反应.故答案为:Ca(OH)2+2HCl═CaCl2+2H2O,红色逐渐褪去;
(3)最终观察到废液呈浑浊状,原因是其中含白色沉淀碳酸钙;废液过滤,滤液中一定含有氯化钠;若滤液呈无色,则一定呈中性,不可能为呈酸性,原因是废液中含碳酸钙,不可能还含酸;若该滤液呈红色,则溶液呈碱性,能使溶液呈碱性的物质可能是:氢氧化钙;氢氧化钠;碳酸钠;或碳酸钠和氢氧化钠;或氢氧化钠和氢氧化钙.如果产生白色沉淀,溶液仍为红色,那么猜想三正确;故答案为:CaCO3;①NaCl; ②废液中含碳酸钙,不可能还含酸;③碳酸钠(或氢氧化钠和氢氧化钙).
解答:解:(1)甲实验中盐酸和氢氧化钙反应生成氯化钙和水,配平即可;当观察到甲中出现红色逐渐褪去时,证明恰好完全反应.故答案为:Ca(OH)2+2HCl═CaCl2+2H2O,红色逐渐褪去;
(3)最终观察到废液呈浑浊状,原因是其中含白色沉淀碳酸钙;废液过滤,滤液中一定含有氯化钠;若滤液呈无色,则一定呈中性,不可能为呈酸性,原因是废液中含碳酸钙,不可能还含酸;若该滤液呈红色,则溶液呈碱性,能使溶液呈碱性的物质可能是:氢氧化钙;氢氧化钠;碳酸钠;或碳酸钠和氢氧化钠;或氢氧化钠和氢氧化钙.如果产生白色沉淀,溶液仍为红色,那么猜想三正确;故答案为:CaCO3;①NaCl; ②废液中含碳酸钙,不可能还含酸;③碳酸钠(或氢氧化钠和氢氧化钙).
| 实验内容 | 现象 | 结论 |
| 取少量滤液于试管中,加入过量Ca(NO3)2溶液,静置 | 产生白色沉淀,溶液仍为红色 | 第三组同学的猜想正确 |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目