题目内容
熟记“部分酸、碱、盐的溶解性表”可帮助我们解决许多化学问题:
①用水可以一次性鉴别出:氢氧化钠、氧化钙、碳酸钙、硝酸铵这几种白色固体.取等量的样品,加入适量的水后,确证硝酸铵的现象是 ;
确证氧化钙的现象是 ;
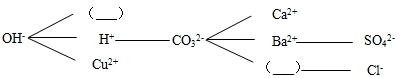
②根据酸、碱、盐三类物质间的反应规律和溶解性,可构建下列离子对,在括号内填写相应的离子符号,要求新构成的两对离子对结合时,一个有气体产生,一个有沉淀生成:
③同学们在实验室探究H2SO4、NaOH与酚酞反应规律后,将废液倒入废液缸,最终废液缸中溶液呈红色,则废液缸中除酚酞外,还含有 种溶质.
①用水可以一次性鉴别出:氢氧化钠、氧化钙、碳酸钙、硝酸铵这几种白色固体.取等量的样品,加入适量的水后,确证硝酸铵的现象是
确证氧化钙的现象是
②根据酸、碱、盐三类物质间的反应规律和溶解性,可构建下列离子对,在括号内填写相应的离子符号,要求新构成的两对离子对结合时,一个有气体产生,一个有沉淀生成:

③同学们在实验室探究H2SO4、NaOH与酚酞反应规律后,将废液倒入废液缸,最终废液缸中溶液呈红色,则废液缸中除酚酞外,还含有
考点:酸、碱、盐的鉴别,生石灰的性质与用途,中和反应及其应用,铵态氮肥的检验,复分解反应的条件与实质
专题:物质的鉴别题,化学反应的基本类型和能量变化
分析:根据酸、碱、盐的溶解性,要鉴别出不同的物质,水是常用的溶剂,有的物质不溶于水,有的物质溶于水吸热,有的放热,有的无变化,酚酞遇碱性溶液变红色等知识进行分析.
解答:解:①氢氧化钠易溶于水,溶于水放热;氧化钙与水反应放出大量的热,生成的氢氧化钙微溶于水,所以固体不全溶;碳酸钙不溶于水;硝酸铵溶于水吸热,所以确证硝酸铵的现象是:固体溶解,溶液温度降低,确证氧化钙的现象是:固体不全溶,溶液温度升高;
②OH-和NH4+有气体产生,CO32-和Ag+有白色沉淀生成,所以括号内填写相应的离子符号为:NH4+;Ag+;
③酚酞遇碱变红色,所以废液缸中除酚酞外,还含有硫酸钠和氢氧化钠两种溶质.
故答案为:①固体溶解,溶液温度降低,固体不全溶,溶液温度升高;
②NH4+;Ag+;
③2.
②OH-和NH4+有气体产生,CO32-和Ag+有白色沉淀生成,所以括号内填写相应的离子符号为:NH4+;Ag+;
③酚酞遇碱变红色,所以废液缸中除酚酞外,还含有硫酸钠和氢氧化钠两种溶质.
故答案为:①固体溶解,溶液温度降低,固体不全溶,溶液温度升高;
②NH4+;Ag+;
③2.
点评:本题主要考查了酸、碱、盐之间的反应,注意复分解反应条件的应用.

练习册系列答案
相关题目
实验室用高锰酸钾制取氧气的装置中,不需要使用的仪器是( )
| A、酒精灯 | B、铁架台 |
| C、试管 | D、蒸发皿 |
已知某原子核电荷数为a,该原子中核内有b个质子和c个中子,核外有d个电子.则( )
| A、a=b=c |
| B、b=c=d |
| C、a=c=d |
| D、a=b=d |