题目内容
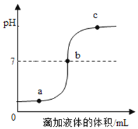
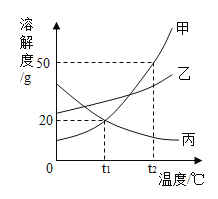
【题目】向一定量Fe2(SO4)3和CuSO4的混合溶液中加入铁粉,搅拌使之充分反应,已知铁粉能与Fe2(SO4)3溶液发生反应:Fe2(SO4)3+Fe=3FeSO4。如图为加入铁粉的质量与烧杯中剩余固体质量关系。下列说法正确的是

A. a点溶液中含有两种溶质
B. m=12.8
C. 取c点固体加入足量稀盐酸,固体全部溶解
D. a点和b点溶液中FeSO4的质量比为3:4
【答案】AD
【解析】
根据在混合物中加入铁粉后,铁会首先与硫酸铁反应生成硫酸亚铁,然后又硫酸铜反应生成硫酸亚铁和铜进行分析。
通过分析图象可知,0---a是铁与硫酸铁反应,参加反应的铁的质量为5.6g,a---b是铁和硫酸铜反应,参加反应的铁的质量5.6g,所以:
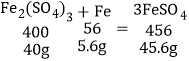
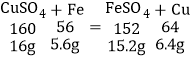
A、a点表示铁与硫酸铁反应恰好反应,溶液中有硫酸铜、硫酸亚铁2种溶质,故A正确;
B、生成铜的质量是6.4g,剩余固体的质量不是12.8g,故B错误;
C、取c点固体为铜和过量的铁粉,加入足量稀盐酸,固体中还有不能溶解的铜,故C错误;
D、a点和b点溶液中FeSO4的质量比为45.6g:(45.6g+15.2g)=3:4,故D正确。
故选AD。

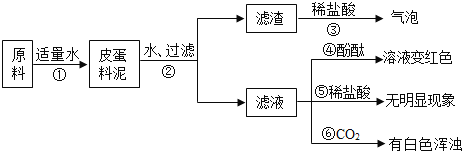
【题目】某实验小组利用石灰石残渣(杂质不溶于水也不溶于酸)制备轻质CaCO3,同时得到K2SO4,其工艺流程简要如下:
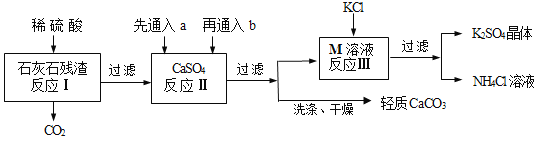
已知:CaCO3 + H2O + CO2 = Ca(HCO3)2
(1)为了提高反应Ⅰ的速率,下列措施中可行的是____(填序号);
①搅拌 ②将残渣粉碎成细小颗粒 ③适当增大硫酸的浓度
(2)反应Ⅱ中a和b分别是____(填序号);
①足量CO2、适量NH3 ②足量NH3、适量CO2
③适量CO2、足量NH3 ④适量NH3、足量CO2
(3)反应Ⅲ中相关物质的溶解度如下表,该表中M物质的化学式为____,反应Ⅲ在常温下能实现的原因是____,生成的NH4Cl溶液在农业上可用作____;
物 质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)将得到的轻质CaCO3进行洗涤,判断CaCO3固体已洗涤干净的方法:取最后一次洗涤液,____(填序号),若无明显的现象,则已洗净;
①滴加稀盐酸
②滴加Na2SO4 溶液
③滴加BaCl2溶液
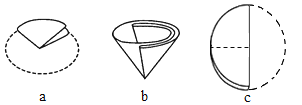
(5)过滤器中的滤纸折叠方法如图所示,正确的顺序是____(填序号);
(6)该工艺流程中可循环利用的物质除H2O外,还有____。