题目内容
 (2006?贵阳)金属是一类重要的材料,人类生产、生活都离不开金属.下面是小明同学对铁的部分知识的学习、探究.
(2006?贵阳)金属是一类重要的材料,人类生产、生活都离不开金属.下面是小明同学对铁的部分知识的学习、探究.(1)查元素周期表,得有关信息如图.则铁原子的核外电子数为
26
26
.(2)钢铁的生产和使用是人类社会进步的一个重要标志.工业上用一氧化碳把赤铁矿(主要成分是Fe2O3)中的铁还原出来的化学方程式为
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
(3)对铁制品生锈的情况进行调查:
| 调查内容 | 脱漆的自行车 | 炒菜的铁锅 | 涂油的无锈铁钉 |
| 铁制品锈蚀的现象 | 风吹雨淋,时间长了脱漆处会生锈 | 清洗后,水擦干不易生锈,水未擦干易生锈 | 较长时间仍不生锈 |
铁制品裸露在潮湿的空气中
铁制品裸露在潮湿的空气中
.(4)为证明铁的金属活动性比铜强,小明设计的实验是
向硫酸铜溶液中插入铁丝
向硫酸铜溶液中插入铁丝
;发生反应的化学方程式为Fe+CuSO4═FeSO4+Cu
Fe+CuSO4═FeSO4+Cu
.分析:原子对外不显电性,因为质子数等于电子数;要得到金属单质可以有多种方法,可以用还原剂还原金属氧化物,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳;钢铁制品在潮湿的空气中容易生锈,因此铁生锈是铁、氧气和水共同作用的结果.证明铁的金属活动性比铜强,可以向硫酸铜溶液中插入铁丝,其它方法也可.
解答:解:(1)原子对外不显电性,因为质子数等于电子数,故答案为:26
(2)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;故答案为:Fe2O3+3CO
2Fe+3CO2
(3)钢铁制品在潮湿的空气中容易生锈,因此铁生锈是铁、氧气和水共同作用的结果;故答案为:铁制品裸露在潮湿的空气中
(4)要证明铁的金属活动性比铜强,可以向硫酸铜溶液中插入铁丝,铁丝表面有红色物质生成;铁和硫酸铜反应生成硫酸亚铁和铜,故答案为:向硫酸铜溶液中插入铁丝;Fe+CuSO4═FeSO4+Cu
(2)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,配平即可;故答案为:Fe2O3+3CO
| ||
(3)钢铁制品在潮湿的空气中容易生锈,因此铁生锈是铁、氧气和水共同作用的结果;故答案为:铁制品裸露在潮湿的空气中
(4)要证明铁的金属活动性比铜强,可以向硫酸铜溶液中插入铁丝,铁丝表面有红色物质生成;铁和硫酸铜反应生成硫酸亚铁和铜,故答案为:向硫酸铜溶液中插入铁丝;Fe+CuSO4═FeSO4+Cu
点评:本考点考查了原子的电中性、一氧化碳的还原性、铁生锈的条件和金属的活动性顺序,属于结合课本知识的信息,并注意化学方程式的配平.还要了解金属生锈的条件和防止金属生锈的措施.本考点主要出现在填空题中.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
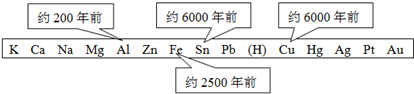 (2006?云南)金属是人类生产生活都离不开的重要材料.根据如图所示人类大规模开发、利用几种金属的大致年代和有关的化学知识,有同学认为对金属大规模开发、利用的先后顺序的影响因素有:
(2006?云南)金属是人类生产生活都离不开的重要材料.根据如图所示人类大规模开发、利用几种金属的大致年代和有关的化学知识,有同学认为对金属大规模开发、利用的先后顺序的影响因素有: