题目内容
暑假过后,同学们在帮老师整理实验室时,发现一瓶久置的敞口石灰石水试剂瓶的瓶壁和瓶塞周围有一些白色粉末,为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
【提出问题】白色粉末的成分是什么
【进行猜想】
猜想一:白色粉末为碳酸钙(请写出碳酸钙产生的化学方程式) .
猜想二:白色粉末为碳酸钙和氢氧化钙的混合物;
猜想三:白色粉末为氢氧化钙(暑假气温较高,由于氢氧化钙的溶解度降低或溶剂蒸发,石灰水中的溶质结晶析出)
【查阅资料】部分碱、盐溶解性表
【设计实验】
(1)甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解.于是他得出粉末中一定有CaCO3的结论.乙同学认为甲同学的结论不严密,理由是
(2)为了得出较严密的结论,他们又进行了如下实验,请完成下列实验报告:
【交流与反思】
(1)通过上述实验的探究,同学们对实验室易变质的溶液时的保存和使用提出了下列建议,其中合理的是 (填序号).
A.密封保存 B.使用前临时配制 C.禁止使用这种试剂.
(2)冰同学又找了一瓶久置的氢氧化钠溶液,取少量溶液样品于试管中,滴加酚酞试液,溶液变红,于是他认为样品中一定会有氢氧化钠,该结论是否正确? (选填“是”或“否”),请说明理由 (3)请你写出另外一种常温下在空气中会变质的药品 .
【提出问题】白色粉末的成分是什么
【进行猜想】
猜想一:白色粉末为碳酸钙(请写出碳酸钙产生的化学方程式)
猜想二:白色粉末为碳酸钙和氢氧化钙的混合物;
猜想三:白色粉末为氢氧化钙(暑假气温较高,由于氢氧化钙的溶解度降低或溶剂蒸发,石灰水中的溶质结晶析出)
【查阅资料】部分碱、盐溶解性表
| 1 | OH- | Cl- | CO32- |
| Ca2+ | 微 | 溶 | 不 |
(1)甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解.于是他得出粉末中一定有CaCO3的结论.乙同学认为甲同学的结论不严密,理由是
(2)为了得出较严密的结论,他们又进行了如下实验,请完成下列实验报告:
| 实 验 步 骤 | 可能观察到的现象 | 猜想二正确 |
| ①取(1)试管中的上层清液,滴加1~2滴无色酚酞试液. | ||
| ②往(1)中试管的残留固体中加入稀盐酸. | 有气泡产生. |
(1)通过上述实验的探究,同学们对实验室易变质的溶液时的保存和使用提出了下列建议,其中合理的是
A.密封保存 B.使用前临时配制 C.禁止使用这种试剂.
(2)冰同学又找了一瓶久置的氢氧化钠溶液,取少量溶液样品于试管中,滴加酚酞试液,溶液变红,于是他认为样品中一定会有氢氧化钠,该结论是否正确?
考点:实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【进行猜想】
氢氧化钙能和空气中的二氧化碳反应生成碳酸钙和水;
【设计实验】
(1)氢氧化钙微溶于水,少量的水中溶解的氢氧化钙很少,因此取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解,不能说明粉末中一定有碳酸钙;
(2)碳酸钙不溶于水,氢氧化钙微溶于水,氢氧化钙的水溶液显碱性,能使酚酞试液变红色;
碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
【交流与反思】
(1)对实验室易变质的溶液应该密封保存,最好是使用前临时配制;
(2)氢氧化钠溶液能够吸收空气中的二氧化碳,并且能和二氧化碳反应生成碳酸钠和水;
通常情况下,氧化钙能和水反应生成氢氧化钙.
氢氧化钙能和空气中的二氧化碳反应生成碳酸钙和水;
【设计实验】
(1)氢氧化钙微溶于水,少量的水中溶解的氢氧化钙很少,因此取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解,不能说明粉末中一定有碳酸钙;
(2)碳酸钙不溶于水,氢氧化钙微溶于水,氢氧化钙的水溶液显碱性,能使酚酞试液变红色;
碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
【交流与反思】
(1)对实验室易变质的溶液应该密封保存,最好是使用前临时配制;
(2)氢氧化钠溶液能够吸收空气中的二氧化碳,并且能和二氧化碳反应生成碳酸钠和水;
通常情况下,氧化钙能和水反应生成氢氧化钙.
解答:解:【进行猜想】
石灰水能够吸收空气中的二氧化碳,并且能和二氧化碳反应生成碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:Ca(OH)2+CO2═CaCO3↓+H2O.
【设计实验】
(1)因为氢氧化钙微溶于水,所以取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解时,不能说明粉末中一定含有碳酸钙,也可能是氢氧化钙.
故填:氢氧化钙微溶于水,不溶解的白色固体可能是氢氧化钙.
(2)如果粉末中含有氢氧化钙,则向试管中的上层清液中滴加无色酚酞试液时,酚酞试液变红色;
如果粉末中含有碳酸钙,则向试管中的残留固体中加入稀盐酸时,会产生气泡.
故填:酚酞试液变红色.
【交流与反思】
(1)对实验室易变质的溶液应该密封保存,或使用前临时配制,但是不能禁止使用这种试剂.
故填:AB.
(2)因为氢氧化钠溶液能够吸收空气中的二氧化碳,氢氧化钠和二氧化碳反应生成的碳酸钠溶液显碱性,也能使酚酞试液变红色,所以取少量溶液样品于试管中,滴加酚酞试液时溶液变红,不能说明样品中一定含有氢氧化钠.
故填:氢氧化钠和二氧化碳反应生成的碳酸钠溶液显碱性,也能使酚酞试液变红色.
(3)常温下氧化钙能和水反应生成氢氧化钙而变质.
故填:氧化钙.
石灰水能够吸收空气中的二氧化碳,并且能和二氧化碳反应生成碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:Ca(OH)2+CO2═CaCO3↓+H2O.
【设计实验】
(1)因为氢氧化钙微溶于水,所以取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解时,不能说明粉末中一定含有碳酸钙,也可能是氢氧化钙.
故填:氢氧化钙微溶于水,不溶解的白色固体可能是氢氧化钙.
(2)如果粉末中含有氢氧化钙,则向试管中的上层清液中滴加无色酚酞试液时,酚酞试液变红色;
如果粉末中含有碳酸钙,则向试管中的残留固体中加入稀盐酸时,会产生气泡.
故填:酚酞试液变红色.
【交流与反思】
(1)对实验室易变质的溶液应该密封保存,或使用前临时配制,但是不能禁止使用这种试剂.
故填:AB.
(2)因为氢氧化钠溶液能够吸收空气中的二氧化碳,氢氧化钠和二氧化碳反应生成的碳酸钠溶液显碱性,也能使酚酞试液变红色,所以取少量溶液样品于试管中,滴加酚酞试液时溶液变红,不能说明样品中一定含有氢氧化钠.
故填:氢氧化钠和二氧化碳反应生成的碳酸钠溶液显碱性,也能使酚酞试液变红色.
(3)常温下氧化钙能和水反应生成氢氧化钙而变质.
故填:氧化钙.
点评:实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质的性质中,属于物质的物理性质的是( )
| A、铜能在潮湿的空气中生成铜绿 |
| B、胆矾溶液反应有蓝色沉淀生成 |
| C、石灰石与稀盐酸反应有二氧化碳气体生成 |
| D、胆矾晶体能碾成粉末 |
化学在人类社会发展中起着重要的作用,请你分析下列四个选项中化学学科不涉及的研究领域是( )
| A、开发新的能源 |
| B、合成新的物质 |
| C、研究物体运动规律 |
| D、防治环境污染 |
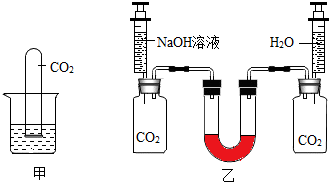 实验小组的同学为了验证氢氧化钠的溶液是否与二氧化碳反应,做了如图所示的实验,像两个装满二氧化碳的同样规格的瓶中分别注入等量的氢氧化钠的溶液和蒸馏水,振荡后放在水平的桌面,观察U形管(装有红墨水)两端液面的变化情况,请问:
实验小组的同学为了验证氢氧化钠的溶液是否与二氧化碳反应,做了如图所示的实验,像两个装满二氧化碳的同样规格的瓶中分别注入等量的氢氧化钠的溶液和蒸馏水,振荡后放在水平的桌面,观察U形管(装有红墨水)两端液面的变化情况,请问: