题目内容
在标准状况下,6.2g磷在氧气中充分燃烧,需要氧气多少升?同时能生成产物的质量为多少克?(已知标准状况下氧气的密度为1.43g/l)
【答案】分析:红磷燃烧是和氧气反应生成了五氧化二磷,根据该反应的化学方程式和红磷的质量,可计算出需要氧气以及生成的五氧化二磷的质量;然后根据密度公式可计算出这些氧气在标准状况下的体积.
解答:解:设6.2g红磷完全燃烧需要氧气的质量为x,生成五氧化二磷的质量为y
4P+5O2 2P2O5
2P2O5
124 160 384
6.2g x y
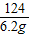 =
= =
=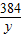
解得:x=8g,y=19.2g
所需氧气的体积为:8g÷1.43g/L=5.6L
答:需要氧气5.6L,同时能生成产物的质量为19.2g.
点评:本题为基础的化学方程式的计算,但由于结合了气体的密度使得本题计算难度扩大,解答时注意密度公式的变形的应用.
解答:解:设6.2g红磷完全燃烧需要氧气的质量为x,生成五氧化二磷的质量为y
4P+5O2
 2P2O5
2P2O5124 160 384
6.2g x y
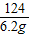 =
= =
=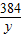
解得:x=8g,y=19.2g
所需氧气的体积为:8g÷1.43g/L=5.6L
答:需要氧气5.6L,同时能生成产物的质量为19.2g.
点评:本题为基础的化学方程式的计算,但由于结合了气体的密度使得本题计算难度扩大,解答时注意密度公式的变形的应用.

练习册系列答案
相关题目