题目内容
某研究性学习小组在协助老师清理实验储备室时,发现一批存放多年的氢氧化钙.为检验其变质情况,进行了如下探究:
(1)学习小组同学取了一定量的样品放入水中充分溶解后,过滤,向滤液中滴加了酚酞溶液,溶液呈红色.由此可得出的结论是:样品中含有 .
(2)小组同学另称取样品20g于锥形瓶中,向锥形瓶中逐滴滴加14.6%的稀盐酸,观察到有气体生成,证明样品中还含有碳酸钙.若将生成的气体收集起来,充分反应后共收集到气体2.2g.
试求样品中碳酸钙的质量分数.
(1)学习小组同学取了一定量的样品放入水中充分溶解后,过滤,向滤液中滴加了酚酞溶液,溶液呈红色.由此可得出的结论是:样品中含有
(2)小组同学另称取样品20g于锥形瓶中,向锥形瓶中逐滴滴加14.6%的稀盐酸,观察到有气体生成,证明样品中还含有碳酸钙.若将生成的气体收集起来,充分反应后共收集到气体2.2g.
试求样品中碳酸钙的质量分数.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据向滤液中滴加了酚酞溶液,溶液呈红色,酚酞遇碱性溶液会变红色,氢氧化钙的溶液显碱性,所以有氢氧化钙解答;
(2)由二氧化碳的质量,根据碳酸钙与稀盐酸反应的化学方程式,可以计算出石灰石中碳酸钙的质量和其质量分数.
(2)由二氧化碳的质量,根据碳酸钙与稀盐酸反应的化学方程式,可以计算出石灰石中碳酸钙的质量和其质量分数.
解答:解:
(1)向滤液中滴加了酚酞溶液,酚酞遇碱性溶液会变红色,氢氧化钙的溶液显碱性,所以有氢氧化钙,说明氢氧化钙没有完全变质.
(2)设石灰石中碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 2.2g
=
x=5g
碳酸钙的质量分数为
×100%=25%
答案:
(1)氢氧化钙
(2)样品中碳酸钙的质量分数25%
(1)向滤液中滴加了酚酞溶液,酚酞遇碱性溶液会变红色,氢氧化钙的溶液显碱性,所以有氢氧化钙,说明氢氧化钙没有完全变质.
(2)设石灰石中碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 2.2g
| 100 |
| 44 |
| x |
| 2.2g |
x=5g
碳酸钙的质量分数为
| 5g |
| 20g |
答案:
(1)氢氧化钙
(2)样品中碳酸钙的质量分数25%
点评:氢氧化钙能与二氧化碳反应生成碳酸钙,而氢氧化钙微溶于水,而碳酸钙难溶于水.利用氢氧化钙与碳酸钙性质的不同,设计实验鉴别两物质是否存在是本题的一个重要考查内容

练习册系列答案
相关题目
2012年11月,佛山市人大常委会执法检查组实地检查发现,本地PM2.5常处于超标状态.PM2.5是指大气中直径小于或等于2.5微米的可吸入颗粒物.下列做法不合理的是( )
| A、举行“地球一小时“熄灯活动 |
| B、鼓励使用太阳能热水器 |
| C、加强建筑工地扬尘控制 |
| D、大力发展火力发电 |
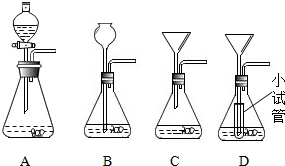 对实验进行改进是创新的表现方式之一.某校科学探究小组的同学用实验室三种漏斗(分液漏斗、长颈漏斗、普通漏斗)装配了A、B、C三套的装置,对固液不加热型气体装置进行探究.请认真分析并回答下列问题:
对实验进行改进是创新的表现方式之一.某校科学探究小组的同学用实验室三种漏斗(分液漏斗、长颈漏斗、普通漏斗)装配了A、B、C三套的装置,对固液不加热型气体装置进行探究.请认真分析并回答下列问题: 在河旁有甲、乙、丙、丁四座工厂(位置如图所示),每个工厂排出的废液只含有Na2CO3、FeCl3、NaOH、HCl中的一种.某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡、河水澄清.乙处排出的物质的化学式是
在河旁有甲、乙、丙、丁四座工厂(位置如图所示),每个工厂排出的废液只含有Na2CO3、FeCl3、NaOH、HCl中的一种.某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡、河水澄清.乙处排出的物质的化学式是 如图A是铝元素在元素周期表中的相关信息,B是其原子结构示意图.
如图A是铝元素在元素周期表中的相关信息,B是其原子结构示意图.