题目内容
铁是工农业生产和人们生活离不开的重要金属材料之一,人类每年都要从自然界的铁矿石中获取大量的铁.铁矿石的种类很多,常见的有黄铁矿、赤铁矿等.(1)上述二种矿石中,人们通常选用赤铁矿石用于铁的冶炼,你认为可能的原因是
(2)现有192吨含Fe2O380%的赤铁矿石,理论上可炼出含铁96%的生铁的质量为
分析:(1)对比两种铁矿石的不同点,分析所选用的矿石的优点;
(2)根据冶炼过程中铁元素的质量不变,利用赤铁矿的质量计算可炼出生铁的质量.
(2)根据冶炼过程中铁元素的质量不变,利用赤铁矿的质量计算可炼出生铁的质量.
解答:解:(1)黄铁矿的主要成分为FeS2,而赤铁矿的主要成分为Fe2O3;两种矿除组成元素明显不同外,其中铁元素的质量分数也不相同:FeS2中Fe的质量分数=
×100%≈46.7%,Fe2O3中Fe的质量分数=
× 100%=70%;
通过以上对比,可推断使用赤铁矿冶炼是因为该铁矿中铁的质量分数高,且不含硫元素冶炼过程中不会产生污染;赤铁矿资源比较广泛;
故答案为:含铁量高,生产过程中污染小或资源广;
(2)解法一:192吨含Fe2O380%的赤铁矿石中含Fe2O3的质量=192吨×80%=153.6吨
153.6吨Fe2O3中含Fe元素质量=153.6吨×70%=107.52吨
则含铁96%的生铁的质量=107.52吨÷96%=112吨
解法二:设生成的质量为x
192吨×80%×70%=x×96%
解之得 x=112吨
故答案为:112.
| 56 |
| 120 |
| 56×2 |
| 160 |
通过以上对比,可推断使用赤铁矿冶炼是因为该铁矿中铁的质量分数高,且不含硫元素冶炼过程中不会产生污染;赤铁矿资源比较广泛;
故答案为:含铁量高,生产过程中污染小或资源广;
(2)解法一:192吨含Fe2O380%的赤铁矿石中含Fe2O3的质量=192吨×80%=153.6吨
153.6吨Fe2O3中含Fe元素质量=153.6吨×70%=107.52吨
则含铁96%的生铁的质量=107.52吨÷96%=112吨
解法二:设生成的质量为x
192吨×80%×70%=x×96%
解之得 x=112吨
故答案为:112.
点评:解法二利用变化前后物质中铁元素质量不变建立方程解决生铁质量和解法一相比,减少了计算量,降低因计算过程多而出现结果误差的几率.

练习册系列答案
相关题目
铁是工农业生产和人们生活离不开的重要金属材料之一.
(1)工业上利用高炉炼铁所需原料有铁矿石、焦炭、石灰石,其中,焦炭的作用是 ①
② ;用一氧化碳和赤铁矿(主要成分氧化铁)反应炼铁的化学方程式 .
(2)通过以上方法得到的是生铁,另一种铁合金的名称是 .
(3)为探究铁钉锈蚀条件,一位同学设计了以下实验:
该同学根据以上实验现象得出了铁钉锈蚀是铁与空气中的氧气、水蒸气等发生化学反应的过程.你认为,该同学的以上实验方案是否合理 (填“合理”或“不合理”),理由是
.
(4)请举出一个防止铁制品生锈的实例
.
(1)工业上利用高炉炼铁所需原料有铁矿石、焦炭、石灰石,其中,焦炭的作用是 ①
②
(2)通过以上方法得到的是生铁,另一种铁合金的名称是
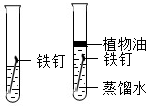
(3)为探究铁钉锈蚀条件,一位同学设计了以下实验:
| 实验一 | 实验二 | |
实验装置 |
 |
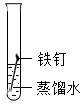 |
| 10天后观察到的实验现象 | 铁钉表面没有明显的锈斑 | 铁钉表面有明显的锈斑 |
(4)请举出一个防止铁制品生锈的实例
 铁是工农业生产和人们生活离不开的重要金属材料之一,人类每年要从自然界获 取大量的铁矿资源.学校从某工厂购进一瓶赤铁矿样品,其标签上的部分内容如图所示,请阅读标签信息后,回答下列问题.
铁是工农业生产和人们生活离不开的重要金属材料之一,人类每年要从自然界获 取大量的铁矿资源.学校从某工厂购进一瓶赤铁矿样品,其标签上的部分内容如图所示,请阅读标签信息后,回答下列问题.