题目内容
6g大理石样品与50g稀盐酸恰好完全反应(杂质不参与反应且不溶于水),生成二氧化碳2.2g。求:反应后溶液中溶质的质量分数(计算结果保留一位小数)。
试题分析:反应后溶液中溶质的质量分数等于溶质的质量除以溶液的质量,反应后的溶质是氯化钙,可通过化学方程式求出;溶液的质量等于加入的物质的质量减去气体的质量;
解:设生成的CaCl2的质量为x,反应的CaCO3的质量为y 。
CaCO3+ 2HCl = CaCl2 + CO2 +H2O
100 111 44
y x 2.2g

x=5.55g y=5g
CaCl2溶液的质量分数为:
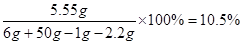
答:所得CaCl2溶液的质量分数为10.5%。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 CaO+CO2↑)
CaO+CO2↑) 2Fe+Al2O3若建设中需要56kg的铁,则消耗铝粉的质量是多少?
2Fe+Al2O3若建设中需要56kg的铁,则消耗铝粉的质量是多少?
