��Ŀ����
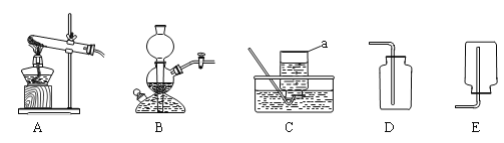
����Ŀ����7�֣�Ϊ����ȡ����֤������̼�����ʣ�����ͬѧ�������ͼʵ��װ�ã������ͼʾ�ش����⣺

��1��װ��A�з����Ļ�ѧ����ʽΪ__________________________________________________��
��2��ʵ�鿪ʼһ��ʱ���װ��B�е���������ɫʯ����Һ______________��ԭ���ǣ��û�ѧ����ʽ���ͣ�____________________________________________________��
��3������ͬѧ�۲쵽װ��C�г���ʯ��ˮ����ǣ��������һ��д����Ӧ�Ļ�ѧ����ʽΪ_______________________________________________________________________��
��4������ͬѧ�۲쵽D���������µ�������Ϩ��˵��CO2���е�������_______________________��
��5����˼����֤������ͬѧ������ʵ��dz��ɹ������룺�����ʵ���B�Թ��еĺ�ɫ��Һ����һ��ʱ�䣬�ֻ���ʲô�����أ����ǣ�����ͬѧ�������ʵ�飬������Һ�ɺ�ɫ��Ϊ_______ɫ������ͬѧ������ԭ����������ͬѧ�û�ѧ����ʽ����ԭ��________________________��
���𰸡���1��CaCO3+2HCl=CaCl2+H2O+CO2��
(2)��� H2O+CO2=H2CO3 (3)CO2+Ca(OH)2=CaCO3��+H2O
(4)�ܶȱȿ��������Ҳ�ȼ����Ҳ��֧��ȼ�� ��5���� H2CO3=H2O+CO2��
��������
�����������1��װ��A���Ǵ���ʯ��ϡ���ᷴӦ�������Ļ�ѧ����ʽΪ��CaCO3+2HCl=CaCl2+H2O+CO2��
(2)������̼����ˮ��Ӧ����̼�ᣬ��ʵ�鿪ʼһ��ʱ���װ��B�е���������ɫʯ����Һ��죬�����Ļ�ѧ��Ӧ����ʽΪ��H2O+CO2=H2CO3
(3) װ��C�г���ʯ��ˮ����ǣ������ڶ�����̼���������Ʒ�����Ӧ����ѧ��Ӧ����ʽΪ��CO2+Ca(OH)2=CaCO3��+H2O
(4) �۲쵽D���������µ�������Ϩ��˵��CO2���е��������ܶȱȿ������Ҳ�ȼ�գ�Ҳ��֧��ȼ��
��5��̼��ȶ������ֽ⣬�ʽ�ʵ���B�Թ��еĺ�ɫ��Һ����һ��ʱ�䣬̼��ֽ���ˣ�����Һ�ɺ�ɫ��Ϊ��ɫ������ʽΪ��H2CO3=H2O+CO2��

����Ŀ��Ϊ�˲ⶨҺ�����б���(C3H8)����������ʱ��ȼ�ղ����һ�����ı������������һ����յ���������ȼ����÷�Ӧǰ������ʵ��������±���
���� | ���� | ���� | ˮ | ������̼ | X |
��Ӧǰ������g | 4.4 | 12.8 | 0 | 0 | 0 |
��Ӧ��������g | 0 | 0 | 7.2 | 4.4 | a |
�����ж���ȷ����
A������a��ֵΪ5��6 B��X�����Ǹ÷�Ӧ�Ĵ���
C��X���ܺ�����Ԫ�� D��Xֻ��̼Ԫ��