题目内容
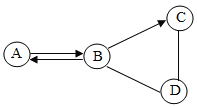
【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列叙述正确的是( )

A. t3℃时,取等质量的三种物质加水使其刚好全部溶解,形成溶液的质量丙>乙>甲
B. t2℃时,20g丙溶解于50g水中能形成70g溶液
C. 分别将三种物质的饱和溶液从t3℃降温至t2℃时,所得溶液溶质质量分数的大小关系为乙>甲=丙
D. 若要将组成在N点的甲溶液转变为M点的甲溶液,可采取添加溶剂的方法
【答案】A
【解析】
A、t3℃时,甲、乙、丙三种物质的溶解度大小为:甲>乙>丙,取等质量的三种物质加水使其刚好全部溶解,需要溶剂的量:丙>乙>甲,故形成溶液的质量丙>乙>甲,符合题意;
B、t2℃时,丙的溶解度为30g,50g水溶解15g丙形成65g溶液,故不符合题意;
C、由图可知,甲、乙的溶解度随温度的升高而增大,丙的溶解度随温度的升高而减小,分别将三种物质的饱和溶液从t3℃降温至t2℃时,丙物质的饱和溶液变为不饱和溶液,质量分数不变,甲、乙的饱和溶液将有固体析出,而且,t2℃时,乙的溶解度比甲的溶解度大即溶质质量分数:乙大于甲,丙溶解的量比甲小,故所得溶液溶质质量分数的大小关系为乙>甲>丙,不符合题意;
D、由图可知,N点在甲曲线的下方,为甲的不饱和溶液,若要将组成在N点的甲溶液转变为M点的甲溶液(甲的饱和溶液),可采取同温度下,添加溶质的方法,故不符合题意。

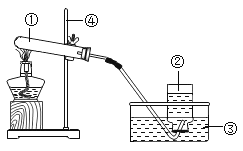
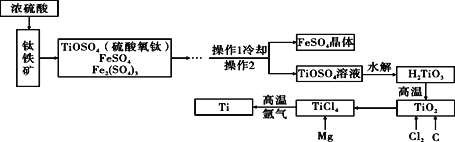
【题目】某兴趣小组对氯酸钾分解反应的催化剂进行研究,在相同的加热条件下完成表中实验:
编号 | 氯酸钾质量/g | 催化剂 | 催化剂质量/g | 收集50mLO2所需时间/s |
实验1 | 5 | ﹣ | ﹣ | 171 |
实验2 | 5 | 二氧化锰 | 0.5 | 49 |
实验3 | 5 | 氧化铁 | 0.5 | 58 |
实验4 | 5 | 氯化钾 | 0.5 | 154 |
(1)设置实验1的目的是____________。
(2)表中所列3种催化剂的催化效果最佳的是_________。
(3)写出实验室用氯酸钾制氧气的文字表达式__________。
(4)由实验1和实验4可知,氯化钾____(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50mLO2,所需时间明显少于171s,解释原因:_____________。
(5)要比较氯酸钾分解反应中不同催化剂的催化效果,除了可以通过测量收集50mLO2所需时间来实现外,还可以通过测量_____________。
【题目】控制变量,设计对比实验是实验探究的重要方法。
实验一:区分硬水和软水。
| 本实验条件除了要控制所取硬、软水的体积相同外,还必须要控制___________相同。 |
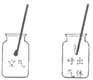
实验二:探究人体吸入的空气与呼出的气体有什么不同。
| 将燃着的小木条分别插入空气样品和呼出气体的样品中,对比观察到的现象,可以得出的结论是___________。 |
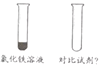
实验三:探究决定氯化铁溶液颜色的粒子。
| 氯化铁溶液呈黄色。为了探究溶液中的哪种粒子使溶液呈黄色,小艳同学分析溶液中存在的粒子,选择了一种试剂作对比,确定了决定氯化铁溶液颜色粒子,用作对比的试剂可以是___________溶液。 |