题目内容
在一次化学课外活动中,小明和小亮做生石灰与水反应的实验时,出现了如下两种不同情况.
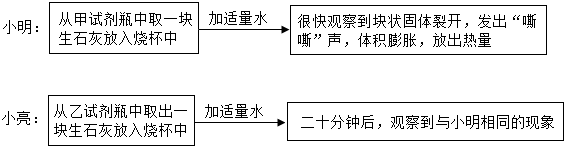
他们经过认真分析后一致认为,小亮的实验出现这种异常情况是由于他所用的生石灰已部分变质.于是分别设计方案如下表,进行实验验证.
请根据以上内容,回答下列问题:
(1)你认为谁的方案不正确?为什么? .
(2)用化学方程式解释生石灰变质的原因 .
(3)乙试剂瓶的固体中一定含有的物质是 .
(4)通过上述实验,你认为保存生石灰时应注意 .

他们经过认真分析后一致认为,小亮的实验出现这种异常情况是由于他所用的生石灰已部分变质.于是分别设计方案如下表,进行实验验证.
| 实验步骤 | 实验现象 | 实验结论 | |
| 小明 | 从乙试剂瓶中取出一块生石灰敲碎后放入烧杯中,加入适量水,然后滴加酚酞溶液 | 酚酞溶液变红 | 存在氢氧化钙,说明样品已部分变质 |
| 小亮 | 从乙试剂瓶中取出一块生石灰,敲碎后放入烧杯中,加入适量稀盐酸 | 有气泡产生 | 存在碳酸钙,说明样品已部分变质 |
(1)你认为谁的方案不正确?为什么?
(2)用化学方程式解释生石灰变质的原因
(3)乙试剂瓶的固体中一定含有的物质是
(4)通过上述实验,你认为保存生石灰时应注意
考点:药品是否变质的探究,生石灰的性质与用途,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:掌握CaO、Ca(OH)2、CaCO3的性质及其相互转化是解题的关键.生石灰的成分为CaO,具有很强的吸水性,还能与空气中的二氧化碳反应变质.
(1)小明用水溶解药品,再加入酚酞溶液,该方法不正确,即使是没有变质的生石灰加水后也会与水反应生成氢氧化钙而使酚酞变红;
(3)小亮同学用乙瓶中试剂做实验,也观察到了体积膨胀放出热量的现象,说明乙瓶中含有CaO,小亮向取出的样品中加盐酸,有气泡产生,说明乙瓶中还含有CaCO3.
(1)小明用水溶解药品,再加入酚酞溶液,该方法不正确,即使是没有变质的生石灰加水后也会与水反应生成氢氧化钙而使酚酞变红;
(3)小亮同学用乙瓶中试剂做实验,也观察到了体积膨胀放出热量的现象,说明乙瓶中含有CaO,小亮向取出的样品中加盐酸,有气泡产生,说明乙瓶中还含有CaCO3.
解答:解:(1)因为生石灰与水反应生成氢氧化钙,也能使酚酞溶液变红,所以不能证明氧化钙已变质,因此小明的方案不正确.
故填:小明的方案不正确,因为生石灰与水反应生成氢氧化钙,也能使酚酞溶液变红,所以不能证明已变质.
(2)氧化钙能和水反应生成氢氧化钙,氢氧化钙能和二氧化碳反应生成碳酸钙和水,反应的化学方程式分别是CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
故填:CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
(3)因为小亮用乙瓶中试剂做实验,也观察到了体积膨胀放出热量的现象,说明乙瓶中含有CaO,小亮向取出的样品中加盐酸,有气泡产生,说明乙瓶中还含有CaCO3.
故填:CaO、CaCO3.
(4)因为生石灰暴露在空气中容易变质,所以应该密封保存.
故填:密封保存.
故填:小明的方案不正确,因为生石灰与水反应生成氢氧化钙,也能使酚酞溶液变红,所以不能证明已变质.
(2)氧化钙能和水反应生成氢氧化钙,氢氧化钙能和二氧化碳反应生成碳酸钙和水,反应的化学方程式分别是CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
故填:CaO+H2O=Ca(OH)2,Ca(OH)2+CO2=CaCO3↓+H2O.
(3)因为小亮用乙瓶中试剂做实验,也观察到了体积膨胀放出热量的现象,说明乙瓶中含有CaO,小亮向取出的样品中加盐酸,有气泡产生,说明乙瓶中还含有CaCO3.
故填:CaO、CaCO3.
(4)因为生石灰暴露在空气中容易变质,所以应该密封保存.
故填:密封保存.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列图象能正确反映所对应实验内容的是( )
A、 向pH=11的NaOH溶液中不断加水 |
B、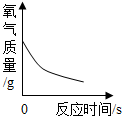 适量MnO2中加人一定量的H2O2溶液 |
C、 可表示硫与氧气反应时的质量关系 |
D、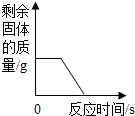 加热KMnO4固体制O2 |
某可燃物X在空气中燃烧的变化如下:X+O2→CO2+H2O则X物质的组成为( )
| A、只含碳元素 |
| B、只含碳、氢两种元素 |
| C、既含碳、氢元素,又含氧元素 |
| D、肯定含碳、氢元素,可能含氧元素 |
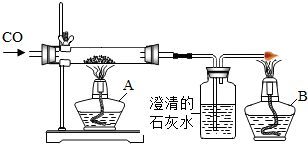
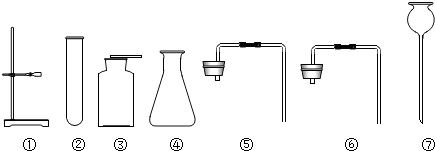
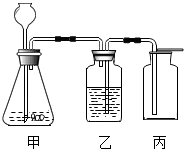 某化学兴趣小组的同学设计了如图所示实验装置,进行气体的制取与收集实验.
某化学兴趣小组的同学设计了如图所示实验装置,进行气体的制取与收集实验.