题目内容
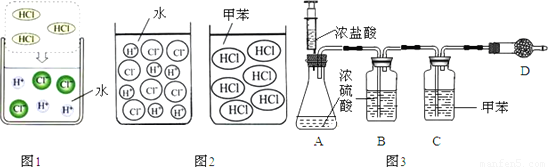
27.Ⅰ、在10%的硫酸溶液中存在着自由移动的微粒是______(填微粒符号),它能和l0%的氢氧化钠溶液发生______反应(填反应类型),反应过程中不断减少的微粒是______(填微粒符号).当两者恰好完全反应时,两种溶液中溶质的计量数之比等于______(用恰当的符号表示).Ⅱ、盐酸是氯化氢(HCl)气体溶于水形成的溶液,HCl是极易溶于水的无色气体.图1为HCl气体溶于水的微观示意图.HCl气体也可溶于甲苯(一种有机溶剂),得氯化氢的甲苯溶液.
某化学兴趣小组的同学对氯化氢与盐酸的化学性质是否相同进行了探究,请你参与探究过程.
[提出问题]氯化氢气体与盐酸的化学性质是否相同?
[查阅资料]
①氯化氢气体是由氯化氢分子构成的;
②在盐酸中存在氢离子、氯离子和水分子;
③氯化氢的甲苯溶液中氯化氢以分子的形式存在.
盐酸与氯化氢的甲苯溶液的微观示意图2所示.
[分析猜想]氯化氢与盐酸的化学性质不一致.进行以上猜想的理由是:______.
[实验准备]为探究氯化氢与盐酸的化学性质,根据实验方案准备时发现缺少氯化氢的甲苯溶液.化学兴趣小组的同学向老师求助,老师用图3所示装置和有关试剂为兴趣小组制取了氯化氢的甲苯溶液.晴晴同学在协助老师制氯化氢的甲苯溶液时产生了疑问,请帮助解答.
(1)为什么浓盐酸加到浓硫酸中能产生大量的氯化氢气体?答:______.
(2)B装置中浓硫酸的作用是什么?答:______.
(3)D中装有用实验室常见的某种物质浓溶液浸湿的棉花,老师说其目的是除去尾气中的氯化氢,反应只生成盐和水.该物质是什么呢?答:______.
[进行实验]用盐酸和氯化氢的甲苯溶液进行对比实验.
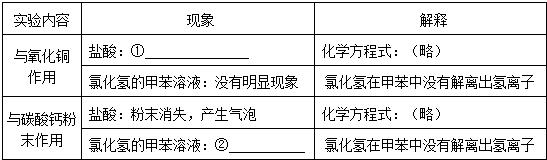
| 实验内容 | 现象 | 解释 |
| 与氧化铜作用 | 盐酸:① | 化学方程式:(略) |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢在甲苯中没有解离出氢离子 | |
| 与碳酸钙粉末作用 | 盐酸:粉末消失,产生气泡 | 化学方程式:(略) |
| 氯化氢的甲苯溶液:② | 氯化氢在甲苯中没有解离出氢离子 |
【答案】分析:根据已有的知识进行分析,酸在水中能电离出自由移动的氢离子和酸根离子,酸碱中和的实质是酸中的氢离子和碱电离出的氢氧根离子结合生成水,浓硫酸具有吸水性,气体在水中的溶解度与温度有关,温度越高,气体的溶解度越小.
解答:解:Ⅰ、在硫酸溶液中,硫酸在水的作用下发生电离,电离出自由移动的氢离子和硫酸根离子,水是由水分子构成的,所以含有氢离子、硫酸根离子和水分子,酸和碱能发生复分解反应,酸碱中和的实质是氢离子和氢氧根离子结合生成水分子,反应后氢离子和氢氧根离子减少,钠离子和硫酸根离子数量不变,其个数比为2:1,所以本题答案为:H+、SO42-、
H2O,复分解,H+、OH-,υ(H2SO4):υ(NaOH)=1:2;
Ⅱ、分析与猜想:盐酸中存在自由移动的氢离子和氯离子,还存在水分子,而氯化氢中只存在自由移动的氯化氢分子,构成微粒不同,性质不同,所以本题答案为:它们的微观构成不同,所以化学性质不同;
(1)浓硫酸具有吸水性,当浓盐酸加入浓硫酸时,浓硫酸吸收水,温度升高,氯化氢在水中的溶解度变小,使盐酸更浓,更容易挥发,故填:浓硫酸吸收水,温度升高,氯化氢在水中的溶解度变小,使盐酸更浓,更容易挥发;
(2)浓硫酸具有吸水性,能除去氯化氢中混有的水蒸气,故填:除去氯化氢气体中的水蒸气,
(3)能和氯化氢反应生成盐和水,装置中的物质是氢氧化钠,故填:NaOH;
①因为盐酸能和氧化铜反应生成氯化铜和水,氯化铜溶液显蓝色,故填:黑色粉末溶解,溶液呈蓝色;
②氯化氢的甲苯溶液不能和碳酸钙反应,故填:没有明显现象.
点评:本题主要考查了常见物质的电离、酸碱中和反应、盐酸和氯化氢分子的化学性质等方面的内容,完成此题,可以依据题干提供的信息结合已有的知识进行.
解答:解:Ⅰ、在硫酸溶液中,硫酸在水的作用下发生电离,电离出自由移动的氢离子和硫酸根离子,水是由水分子构成的,所以含有氢离子、硫酸根离子和水分子,酸和碱能发生复分解反应,酸碱中和的实质是氢离子和氢氧根离子结合生成水分子,反应后氢离子和氢氧根离子减少,钠离子和硫酸根离子数量不变,其个数比为2:1,所以本题答案为:H+、SO42-、
H2O,复分解,H+、OH-,υ(H2SO4):υ(NaOH)=1:2;
Ⅱ、分析与猜想:盐酸中存在自由移动的氢离子和氯离子,还存在水分子,而氯化氢中只存在自由移动的氯化氢分子,构成微粒不同,性质不同,所以本题答案为:它们的微观构成不同,所以化学性质不同;
(1)浓硫酸具有吸水性,当浓盐酸加入浓硫酸时,浓硫酸吸收水,温度升高,氯化氢在水中的溶解度变小,使盐酸更浓,更容易挥发,故填:浓硫酸吸收水,温度升高,氯化氢在水中的溶解度变小,使盐酸更浓,更容易挥发;
(2)浓硫酸具有吸水性,能除去氯化氢中混有的水蒸气,故填:除去氯化氢气体中的水蒸气,
(3)能和氯化氢反应生成盐和水,装置中的物质是氢氧化钠,故填:NaOH;
①因为盐酸能和氧化铜反应生成氯化铜和水,氯化铜溶液显蓝色,故填:黑色粉末溶解,溶液呈蓝色;
②氯化氢的甲苯溶液不能和碳酸钙反应,故填:没有明显现象.
点评:本题主要考查了常见物质的电离、酸碱中和反应、盐酸和氯化氢分子的化学性质等方面的内容,完成此题,可以依据题干提供的信息结合已有的知识进行.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目