题目内容
960千克三氧化二铁(Fe2O3)与多少千克四氧化三铁(Fe3O4)含有相同质量的铁元素?分析:根据盐酸的质量分数公式分别计算出三氧化二铁和四氧化三铁中铁元素的质量分数,然后根据含有铁元素的质量相同,结合质量分数公式计算即可.
解答:解:三氧化二铁中铁元素的质量分数=
×100%=70%;
四氧化三铁中铁元素的质量分数=
×100%≈72.4%;
960kg×70%÷72.4%≈928.2kg.
答:960千克三氧化二铁(Fe2O3)与928.2千克四氧化三铁(Fe3O4)含有相同质量的铁元素.
| 56×2 |
| 56×2+16×3 |
四氧化三铁中铁元素的质量分数=
| 56×3 |
| 56×3+16×4 |
960kg×70%÷72.4%≈928.2kg.
答:960千克三氧化二铁(Fe2O3)与928.2千克四氧化三铁(Fe3O4)含有相同质量的铁元素.
点评:本题主要考查学生运用化学式和元素的质量分数公式进行计算的能力.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
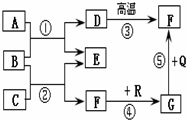 如图是初中化学中常见物质间的转化关系(部分反应条件略去).其中,A、B属于盐,胃酸中含有C,D是石灰石主要成分,F、G是组成元素相同的两种气体,Q、R都是黑色固体,试回答下列问题:
如图是初中化学中常见物质间的转化关系(部分反应条件略去).其中,A、B属于盐,胃酸中含有C,D是石灰石主要成分,F、G是组成元素相同的两种气体,Q、R都是黑色固体,试回答下列问题: