题目内容
现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.取该混合物粉末10g放入烧杯中,将200g 19.6%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 50 | 50 | 50 | 50 |
| 剩余固体的质量/g | 7.6 | 5.2 | 2.8 | 2.4 |
(2)该混合物粉末中另一金属为______
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
解:(1)因铜与酸不反应,反应后剩余固体质量2.4g即为其质量.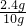 ×100%=24%
×100%=24%
故答案为:24%
(2)每50g稀硫酸可与2.4g这种金属恰好完全反应.设该金属为R,其相对原子质量为r
R+H2SO4═RSO4+H2↑
r 98
2.4g 50g×19.6%
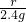 =
=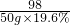
解得:r=24
相对原子质量为24的元素是镁元素.
故答案为:Mg
(3)第三次加入硫酸充分反应后,所用硫酸的质量为150g,反应的金属的质量为10g-2.8g=7.2g.反应后生成的溶质为MgSO4.
设生成MgSO4的质量为x,生成H2的质量为y
Mg+H2SO4═MgSO4+H2↑
98 120 2
150g×19.6% x y

解得:x=36g y=0.6g
C%= ×100%=23.0%
×100%=23.0%
答:所得溶液中溶质的质量分数为23.0%
分析:(1)根据金属活动性顺序,铜与酸不反应,反应后剩余固体质量即为其质量.
(2)每50g稀硫酸可与2.4g这种金属恰好完全反应,根据化学方程式可计算出此金属的相对原子质量.
(3)第三次加入硫酸充分反应后,要确定所得溶液中溶质的种类及溶液的质量.
点评:此题考查金属的活动性顺序,及其化学性质,并能通过化学方程式进行计算.此题中可用差量法计算剩余溶液的质量,即溶液质量=反应的金属质量+反应的酸的质量-生成的气体的质量
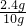 ×100%=24%
×100%=24%故答案为:24%
(2)每50g稀硫酸可与2.4g这种金属恰好完全反应.设该金属为R,其相对原子质量为r
R+H2SO4═RSO4+H2↑
r 98
2.4g 50g×19.6%
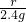 =
=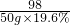
解得:r=24
相对原子质量为24的元素是镁元素.
故答案为:Mg
(3)第三次加入硫酸充分反应后,所用硫酸的质量为150g,反应的金属的质量为10g-2.8g=7.2g.反应后生成的溶质为MgSO4.
设生成MgSO4的质量为x,生成H2的质量为y
Mg+H2SO4═MgSO4+H2↑
98 120 2
150g×19.6% x y

解得:x=36g y=0.6g
C%=
 ×100%=23.0%
×100%=23.0%答:所得溶液中溶质的质量分数为23.0%
分析:(1)根据金属活动性顺序,铜与酸不反应,反应后剩余固体质量即为其质量.
(2)每50g稀硫酸可与2.4g这种金属恰好完全反应,根据化学方程式可计算出此金属的相对原子质量.
(3)第三次加入硫酸充分反应后,要确定所得溶液中溶质的种类及溶液的质量.
点评:此题考查金属的活动性顺序,及其化学性质,并能通过化学方程式进行计算.此题中可用差量法计算剩余溶液的质量,即溶液质量=反应的金属质量+反应的酸的质量-生成的气体的质量

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.取该混合物粉末10g放入烧杯中,将200g 19.6%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
求:(1)该混合物粉末中铜的质量分数为
(2)该混合物粉末中另一金属为
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 50 | 50 | 50 | 50 |
| 剩余固体的质量/g | 7.6 | 5.2 | 2.8 | 2.4 |
(2)该混合物粉末中另一金属为
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.
【查阅资料】(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气.
(2)相对原子质量:Mg-24、Fe-56、Zn-65
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
通过计算(写出计算过程),求:
(1)该混合物粉末中铜的质量分数?
(2)该混合物粉末中另一金属为何种金属?
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
【查阅资料】(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气.
(2)相对原子质量:Mg-24、Fe-56、Zn-65
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.O | 35.0 | 35.O | 35.O |
| 剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
(1)该混合物粉末中铜的质量分数?
(2)该混合物粉末中另一金属为何种金属?
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.
【查阅资料】(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气.
(2)相对原子质量:Mg-24、Fe-56、Zn-65
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
通过计算(写出计算过程),求:
(1)该混合物粉末中铜的质量分数?
(2)该混合物粉末中另一金属为何种金属?
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
【查阅资料】(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气.
(2)相对原子质量:Mg-24、Fe-56、Zn-65
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.O | 35.0 | 35.O | 35.O |
| 剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
(1)该混合物粉末中铜的质量分数?
(2)该混合物粉末中另一金属为何种金属?
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
(2008?攀枝花)现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.
【查阅资料】(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气.
(2)相对原子质量:Mg-24、Fe-56、Zn-65
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
通过计算(写出计算过程),求:
(1)该混合物粉末中铜的质量分数?
(2)该混合物粉末中另一金属为何种金属?
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?
【查阅资料】(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气.
(2)相对原子质量:Mg-24、Fe-56、Zn-65
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.O | 35.0 | 35.O | 35.O |
| 剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
(1)该混合物粉末中铜的质量分数?
(2)该混合物粉末中另一金属为何种金属?
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?