题目内容
【题目】实验是科学探究的重要途径。
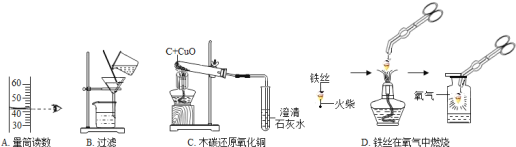
(1)①下列实验仪器不能用于加热的是_______(填字母代号)。
a.烧杯 b.量筒 c.试管 d.蒸发皿
②做铁丝在氧气中燃烧实验时,集气瓶中预先加少量水或铺一层细沙的目的是___________?
③配制质量分数为5%的NaCl溶液,若量取水时仰视量筒读数(其他操作都正确),所得溶液的质量分数________5%(填“大于”、“小于”或“等于”)。
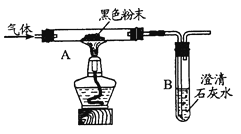
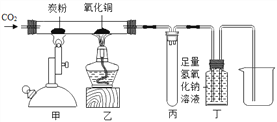
(2)实验室选用以下装置制取纯净、干燥的CO2,并验证其部分性质。
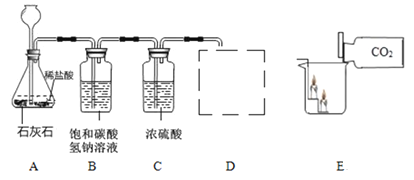
①B装置中发生反应的化学方程式为______________________________________。
②C装置中浓硫酸的作用是___________________。
③请在D中简要补画出CO2的收集装置图。 ________________
④由E可验证CO2具有哪些性质?________________
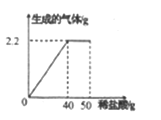
(3)取12.5 g石灰石于装置A中,向其中加入100 g足量的稀盐酸,充分反应后(杂质不参加反应),A中固液混合物的质量为108.1 g,请计算该石灰石中碳酸钙的质量分数________________。
【答案】 b 防止溅落的熔融物炸裂瓶底 小于 NaHCO3+HCl=NaCl+H2O+CO2↑ 干燥气体 ![]() 密度比空气大,不燃烧也不支持燃烧 80%
密度比空气大,不燃烧也不支持燃烧 80%
【解析】(1)①烧杯在加热时需要垫上石棉网,试管和蒸发皿可直接加热,量筒不能加热;②做铁丝在氧气中燃烧实验时,由于铁燃烧放出了大量的热,集气瓶中预先加少量水或铺一层细沙的目的是:防止溅落的熔化物炸裂瓶底;③量取水时仰视凹液面最低处,会使得量取水的体积偏大,则所得溶液的溶质质量分数就好偏小;(2)①B装置中,碳酸氢钠和稀盐酸中挥发出的氯化氢反应生成氯化钠、水和二氧化碳,发生反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;②C装置中浓硫酸的作用是吸收水蒸气;③二氧化碳密度比空气大,可以用向上排空气法收集,如下图所示:![]() ;④此实验的现象是:下层的蜡烛先熄灭,上层的蜡烛后熄灭,说明二氧化碳密度比空气大,不燃烧也不支持燃烧;
;④此实验的现象是:下层的蜡烛先熄灭,上层的蜡烛后熄灭,说明二氧化碳密度比空气大,不燃烧也不支持燃烧;
(3)解:设石灰石中碳酸钙的质量为x,生成二氧化碳的质量为:100 g+12.5 g-108.1 g=4.4 g,
CaCO3+2HCl═CaCl2+CO2↑+H2O,
100 44
x 4.4g
![]()
x=10g,
石灰石中碳酸钙的质量分数为: ![]() ×100%=80%,
×100%=80%,
答:石灰石中碳酸钙的质量分数为80%。

 名校课堂系列答案
名校课堂系列答案